题目内容
【题目】某同学设计对比实验(如图):两个体积相同且均装满二氧化碳的锥形瓶,气球上端的玻璃管与外界大气相通。操作:分别向两锥形瓶中滴入2mL的氢氧化钠溶液和水,轻轻振荡。
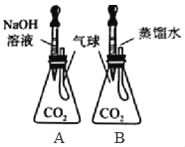
(1)设计该对比实验的目的是_____
(2)现象:观察到A、B两瓶内气球的变化情况是:_____。
(3)B中发生的化学反应方程式为_____。
【答案】证明二氧化碳可以和氢氧化钠反应 A中气球变大,B中气球先变大再变小 CO2+H2O=H2CO3
【解析】
(1)A和B中的区别是A中含有氢氧化钠,实验的目的是证明二氧化碳可以和氢氧化钠反应;
(2)由于A中二氧化碳和氢氧化钠反应生成碳酸钠和水,锥形瓶内气压变小,在外界大气压的作用下气球胀大,B中二氧化碳和水反应生成碳酸,锥形瓶内气压变小,气球胀大,振荡后,碳酸分解成水和二氧化碳,锥形瓶内气压增大,气球变小。所以现象是:A中气球变大,B中气球先变大再变小;
(3)B中二氧化碳和水反应生成碳酸,方程式为:CO2+H2O=H2CO3。

【题目】某初中化学兴趣小组的四位同学,往氢氧化钠溶液中滴入酚酞溶液时,发现溶液变成了红色,可是过了一会儿红色就消失了,溶液恢复为无色。溶液的红色为什么会变成无色呢?他们对这一现象进行了探究。
(提出猜想)
甲:可能是酚酞变质造成的;
乙:可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故;
丙:可能是酚酞与空气中的氧气反应,使红色消失;
丁:可能与氢氧化钠溶液浓度过大有关。
(理论分析)
(1)对于乙同学的猜想,大家认为是不正确的。因为_______,所以红色不会消失。
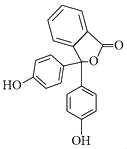
(查阅资料)为了排除是酚酞溶液导致的原因,同学们决定重新配制酚酞溶液进行实验,他们在网络上查阅了资料,百度百科中对酚酞的描述如表:
中文名 | 酚酞 | 结构式 |
|
外观 | 白色至微黄色结晶性粉末 | ||
常温下溶解性 | <0.1g/100mL(水中) >5g/100mL(乙醇中) | ||
化学式 | C20H14O4 |
(2)由上表可知,配制酚酞溶液的溶剂是_______(选填“水”或“乙醇”)。在检验溶液酸碱性的实验中,往待测溶液中滴入1~2滴酚酞溶液即可,滴入过多的酚酞有可能出现白色浑浊的现象,该现象产生的原因是_______。
(实验验证)
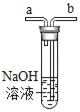
(3)为了验证丙同学的猜想,四位同学在一支密闭的装有NaOH溶液的试管中,先通入密度比空气大的稀有气体,将试管内的空气排尽,随后注入新配制的酚歌试液,观察到的现象依然是溶液先变成红色,过了一会儿红色消失。如图稀有气体应由导管口_______(选“a”或b”)处通入。
(4)若丁同学的猜想正确,请你完成下列实验设计。
实验方法 | 实验现象和结论 |
_______ | _______ |
(应用拓展)
(5)从查阅百度百科资料知道,酚酞(以H2In表示)其实是一种极弱的酸,其遇碱变红的变化表达式为:H2In![]() In2﹣ (红色)。
In2﹣ (红色)。
根据上述信息,请写出H2In遇NaOH溶液变红的化学方程式:_______。
【题目】李呈同学想通过实验,探究某企业用氨碱法生产纯碱样品的成分及含量.
(提出问题)该纯碱样品中含有哪些物质?
(猜想与假设)通过分析,李呈同学做出如下假设:(1)只含有Na2CO3;(2)含有Na2CO3和NaHCO3
(查阅资料)
NaHCO3 | Na2CO3 | |
加入稀盐酸 | 现象I | 产生气泡 |
加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
(1)表中的现象I为________________;
(2)现象Ⅱ对应的化学方程式为____________________.
(实验探究)为了确定纯碱样品的成分,李呈同学设计如下实验方案,请你一起完成下列实验报告.
实验步骤 | 实验现象 | 实验结论及化学方程式 |
A取少量样品溶于水,加入过量的CaCl2溶液 | ①_________________ | 该反应的方程式:②___________ |
B将上述反应后的混合液过滤,取滤液③ _______________ | ④________________ | 证明猜想②成立 |
(注意:正确回答下列问题加4分,总分不超过60分)
(实验反思)实验步骤A中,氯化钙溶液过量的目的是____________.
(提出问题2)如何测量该纯碱样品中各物质的含量?
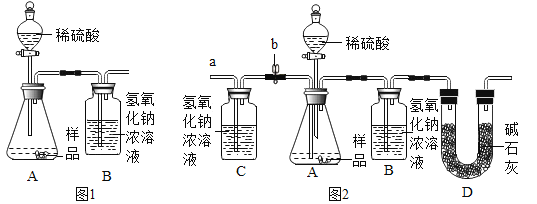
(1)为测量该纯碱样品各成分的含量,毕倭寇同学设了图1装置,通过称量B装置中质量变化来确定样品中各成分的含量.该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误,但多次实验发现,测定结果有偏差.造成偏差的原因有①__________;②______________(2)李呈同学在老师的指导下重新设计了如图2所示的实验装置.该实验有以下操作步骤:
①查装置气密性,将Wg干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
⑥打开活塞b从导管a处缓缓鼓入一定量的空气,关闭活塞b;
⑦根据B瓶增加的质量,计算样品中各成分的含量.该实验的正确步骤是________________.