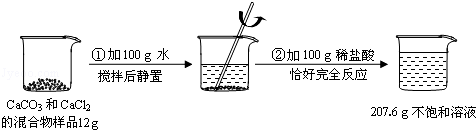
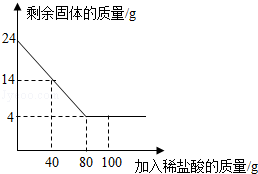
题目内容
在稀硫酸和硫酸铜的混合溶液中,加入适量铁粉,使其恰好反应。,.则原混合溶液中硫酸和硫酸铜的质量比为
| A.7:80 | B.1:1 | C.7:40 | D.49:80 |
A
试题分析:铁与稀硫酸反应使得加入的固体质量减少,铁与硫酸铜溶液反应生成铜,使得加入的固体质量增加,由题目“反应后得到的固体质量与所加铁粉质量相等”知:与稀硫酸、硫酸铜反应的铁的质量总和和与硫酸铜溶液反应生成的铜的质量相等。
全题假设反应生成铜64g.。
1.根据下列化学方程式可求出与硫酸铜反应掉的铁的质量X,硫酸铜的质量Y
Fe+CuSO4=Cu+FeSO4
56 160 64
X Y 64g
X =56g Y=160g
2.由此可知:与稀硫酸反应的铁的质量为64-56=8g,再根据下列化学方程式可计算出稀硫酸的质量M
Fe+H2SO4=FeSO4+H2↑
98
8g M
M=14g
3.所以原混合溶液中硫酸和硫酸铜的质量比为14:160,即7:80,所以A正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目