��Ŀ����
����Ŀ��ˮ�ͽ���������������������о��й㷺����;��
��1������ˮӲ�ȹ����Ӱ�����������Ӧ������ʹ�ã�
a������Ӳˮ���õ������� ��
b�����ij����ˮ�ơ�þ���Ӻ������ߣ�������Ҫ�� CaCl2��MgCl2��ʽ���ڣ������ȼ�����������ʯ�ң���Ӧ�Ļ�ѧ����ʽΪ �� �ټ��������������ɳ���̼��ƣ����ɽ�ˮ������
��2���������֪ʶ��ѧϰ��������벢�ش����⣺
������Ʒ�У���Ҫ���ý��������Ե���������ţ���ͬ��
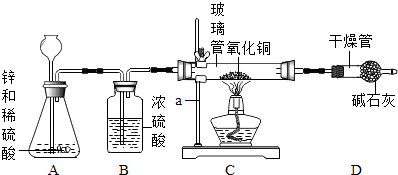
��3������ԭ�ӽṹʾ��ͼΪ  ����ԭ���ڻ�ѧ��Ӧ��������á���ʧ�������ӣ��γɵ����ӷ���Ϊͭ��ϡ�����Ӧ����Ũ������һ�������¿��Է�Ӧ���仯ѧ����ʽΪ��Cu+2H2SO4��Ũ��
����ԭ���ڻ�ѧ��Ӧ��������á���ʧ�������ӣ��γɵ����ӷ���Ϊͭ��ϡ�����Ӧ����Ũ������һ�������¿��Է�Ӧ���仯ѧ����ʽΪ��Cu+2H2SO4��Ũ�� ![]() CuSO4+X��+2H2O����X�Ļ�ѧʽΪ ��
CuSO4+X��+2H2O����X�Ļ�ѧʽΪ ��
���𰸡�
��1���÷���ˮ,MgCl2+Ca��OH��2=Mg��OH��2��+CaCl2,̼����
��2��B
��3��ʧ,Al3+,SO2
���������⣺��1��a������Ӳˮ����ˮ�ķ����ǣ��÷���ˮ���������ˮ����ĭ�������ˮ����ĭ�ٵ���Ӳˮ��
b�����ij����ˮ�ơ�þ���Ӻ������ߣ�������Ҫ�� CaCl2��MgCl2��ʽ���ڣ������ȼ�����������ʯ�ң���Ӧ�Ļ�ѧ����ʽΪ��MgCl2+Ca��OH��2=Mg��OH��2��+CaCl2���ټ���������̼���ƺ����ɳ���̼��ƣ����ɽ�ˮ��������3��������ԭ�ӽṹʾ��ͼ��֪��������������3��С��4����ԭ���ڻ�ѧ��Ӧ����ʧ���ӣ��γ������ӣ�����ΪAl3+���ڷ�Ӧ�Ļ�ѧ����ʽCu+2H2SO4 ![]() CuSO4+X��+2H2O�У���Ӧ����ͭ���⡢����ԭ�Ӹ����ֱ�Ϊ1��4��2��8����Ӧ�����������ͭ���⡢����ԭ�Ӹ����ֱ�Ϊ1��4��1��6�����ݷ�Ӧǰ��ԭ�����ࡢ��Ŀ���䣬��X�к���1����ԭ�Ӻ�2����ԭ�ӣ�������X�Ļ�ѧʽΪSO2��
CuSO4+X��+2H2O�У���Ӧ����ͭ���⡢����ԭ�Ӹ����ֱ�Ϊ1��4��2��8����Ӧ�����������ͭ���⡢����ԭ�Ӹ����ֱ�Ϊ1��4��1��6�����ݷ�Ӧǰ��ԭ�����ࡢ��Ŀ���䣬��X�к���1����ԭ�Ӻ�2����ԭ�ӣ�������X�Ļ�ѧʽΪSO2��
���Դ��ǣ���1��a���÷���ˮ��b��MgCl2+Ca��OH��2=Mg��OH��2��+CaCl2��̼���ƣ���3��ʧ��Al3+��SO2��
�����㾫����������Ҫ������Ӳˮ����ˮ�ͽ������������ʼ���;�����֪ʶ�㣬��Ҫ����Ӳˮ����ˮ�ļ������÷���ˮ���и�����������ĭ���ٵ���Ӳˮ����ĭ�϶������ˮ���������������ʣ� ��1��������һ��Ϊ��̬����ΪҺ̬�����н�������2�������������ɫ��ͭΪ�Ϻ�ɫ����Ϊ��ɫ����3�������õĵ����ԡ������ԡ���չ�Բ�����ȷ�����⣮

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ͼAΪ̼��ԭ����ͭ��ʵ��װ��ͼ����ʦָ����Ӧ�ﲻͬ�������ȿ��ܻ�Ӱ�������������,��ѧϰʱ,���ԴӶ��Թ۲�Ͷ������������Ƕ����ж���������������ʦ��˼·,̽��̼��ԭ����ͭ���ɵ�����.(Ũ���������ˮ��)
��������⡿��̼��ԭ����ͭ���ɵ�������ʲô?
���������롿���������CO �������CO2�������__________
��ʵ����ơ���װ��ͼ��ͼ��
����һ���Ӷ��Թ۲�Ƕ��жϣ�
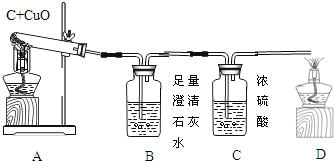
(1)������3����
����B����������___________________
��D��������Ӧ�Ļ�ѧ��Ӧ����ʽ___________________________
���������Ӷ�������Ƕ��жϣ�
�ⶨ�����е��ĸ����ݣ�
��Ӧǰ������ | ��Ӧ������� | |
װ��A | m1 | m2 |
װ��B | m3 | m4 |
��������ڳ���,��m4m3___m1m2(ѡ����>������<������=��)����ʱA�е�������__________________��B������Ӧ�Ļ�ѧ����ʽΪ _________________________
��ʵ�ʲ�����B���ӵ�����С������ֵ������������ܵ�ԭ��__________________________