题目内容
【题目】实验探究一:小明学习了过氧化氢溶液分解知识后,脑洞大开,还想寻找新的催化剂,于是设计了如下探究方案.
(提出问题)红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
(实验探究)
实验步骤 | 实验现象 | 实验结论及解释 |
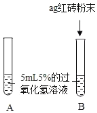
Ⅰ. | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是______; ②红砖粉末能改变过氧化氢分解速率 |
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的_____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
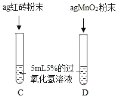
Ⅲ. | 两试管中均产生气泡且 ________ | 红砖粉末的催化效果没有二氧化锰粉末好 |
请写出红砖粉末(成分以Fe2O3表示)催化过氧化氢溶液分解反应的符号表达式_______。
⑵实验探究二:小明继续探究带火星的木条在不同体积分数氧气中的复燃情况,部分实验数据记录如表:
氧气体积分数(%) | 30 | 40 | 60 | 70 |
带火星的木条 | 不变 | 稍亮 | 复燃 | 复燃 |
①根据上述实验数据得出的结论是_____________。
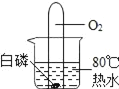
②在集气瓶中注入占其容器50%的水(如图![]() ),用排水法收集氧气,将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,推测实验现象并说明理由:_________。
),用排水法收集氧气,将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,推测实验现象并说明理由:_________。
③配合实验的小林发现双氧水分解也可用氧化铜(难溶于水固体)作催化剂。在0.5g氧化铜中滴加双氧水,反应结束后固体质量为_________________g。
④请你设计一个实验,证明在双氧水分解反应后,氧化铜化学性质没有发生改变。
步骤 | 现象 | 结论 |
_____ | _____ | 氧化铜化学性质没有改变 |
【答案】氧气 质量和化学性质 加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的快 H2O2 ![]() H2O+O2 能使带火星的小木条复燃的不一定是纯氧 带火星的木条复燃,这是因为氧气的浓度达到了使其复燃的纯度 0.5g 将反应后的混合物过滤,向盛有该滤渣的试管中重新加入2mL过氧化氢溶液 试管中有大量气泡冒出,且能使带火星的木条复燃
H2O+O2 能使带火星的小木条复燃的不一定是纯氧 带火星的木条复燃,这是因为氧气的浓度达到了使其复燃的纯度 0.5g 将反应后的混合物过滤,向盛有该滤渣的试管中重新加入2mL过氧化氢溶液 试管中有大量气泡冒出,且能使带火星的木条复燃
【解析】
实验探究一:
[实验探究]
根据氧气能使带火星的木条复燃,可知该气体是氧气,故填氧气;
催化剂能改变化学反应速率,而本身的质量和化学性质在化学反应前后都不变,故填质量和化学性质;
根据红砖粉末的催化效果没有二氧化锰粉末好,可知加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的快,故填加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的快;
红砖粉末(成分以Fe2O3表示)催化过氧化氢溶液分解生成水和氧气,符号表达式故填H2O2 ![]() H2O+O2;
H2O+O2;
实验探究二:
①根据表格数据以及实验现象分析可知,氧气浓度达到60%就能使带火星的小木条复燃,故填能使带火星的小木条复燃的不一定是纯氧;
②假设容器体积为V,在集气瓶中注入占其容器50%的水,用排水法收集氧气,将瓶内的水排尽,可知瓶内氧气体积为50%V+50%V×21%=60.5%V,瓶内氧气浓度为![]() =60.5%,用带火星的木条在该集气瓶中进行实验,由于氧气浓度已经达到能使带火星木条复燃的纯度(60%),会观察到带火星的木条复燃,故填带火星的木条复燃,这是因为氧气的浓度达到了使其复燃的纯度;
=60.5%,用带火星的木条在该集气瓶中进行实验,由于氧气浓度已经达到能使带火星木条复燃的纯度(60%),会观察到带火星的木条复燃,故填带火星的木条复燃,这是因为氧气的浓度达到了使其复燃的纯度;
③催化剂能改变化学反应速率,而本身的质量和化学性质在化学反应前后都不变,反应中氧化铜做催化剂,反应前后质量不变,故填0.5g;
④根据催化剂反应前后化学性质不变,将反应后的混合物过滤,向盛有该滤渣的试管中重新加入2mL过氧化氢溶液后,试管中仍有大量气泡冒出,且能使带火星的木条复燃,从而得出氧化铜的化学性质在化学反应前后没有发生改变的结论,实验步骤故填将反应后的混合物过滤,向盛有该滤渣的试管中重新加入2mL过氧化氢溶液;实验现象故填试管中有大量气泡冒出,且能使带火星的木条复燃。