题目内容
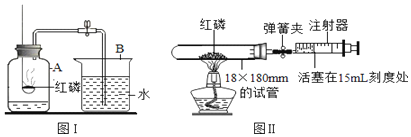
【题目】为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且滑润性很好的针筒注射器组成如图的实验装置。假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:

(1)白磷燃烧的化学方程式为_____。
(2)实验前,打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回20mL刻度处,则说明:_____。
(3)若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等到试管冷却后再松开弹簧夹。可观察到注射器活塞停留在_____mL刻度处。
(4)若不使用弹簧夹,用酒精灯加热白磷,充分反应直至燃烧结束,试管冷却。整个实验过程中可观察到的现象为:_____、_____。
(5)若按小华的设想进行实验,实际可能遇到诸多问题而发生危险,造成实验失败,例如:_____。
【答案】4P+5O2 2P2O5 装置的气密性好 12 白磷燃烧,产生白烟 活塞先向右移动,最终稳定在约8mL的刻度线上 橡胶塞弹出、试管爆裂、注射器活塞弹出等
2P2O5 装置的气密性好 12 白磷燃烧,产生白烟 活塞先向右移动,最终稳定在约8mL的刻度线上 橡胶塞弹出、试管爆裂、注射器活塞弹出等
【解析】
本题是测定氧气在空气中的体积分数的实验探究,要把空气中的氧气消耗掉,在本实验中用的是过量的白磷,燃烧后的生成物是固体,不需要占很大的空间。本实验中用的是40mL的试管与实际容积为60mL且润滑性很好的针筒注射器,并且活塞在20mL处,有助于反应结束后计算体积。要使本实验成功,必须注意以下几点:①装置的气密性好;②白磷足量;③必须冷却到室温再读数。还要注意防止试管受热不均或气体体积受热膨胀过大,从而造成试管炸裂。
(1)白磷燃烧生成五氧化二磷,反应的化学方程式为: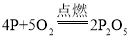 ,故填:
,故填: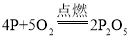 。
。
(2)打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明整个装置都不漏气;故填:装置的气密性好。
(3)若先夹紧弹簧夹,用酒精灯加热白磷,这时白磷燃烧消耗掉的只是试管内的氧气为40mL×1/5=8mL,所以活塞应停在20mL-8mL=12mL的刻度处;故填:12。
(4)若不使用弹簧夹,用酒精灯加热白磷,白磷燃烧,产生白烟,而白磷实际消耗掉的是试管40mL和注射器内20mL的氧气为(40mL+20mL)×1/5=12mL,所以活塞应停在20mL-12mL=8mL的刻度处;故填:白磷燃烧,产生白烟;活塞先向右移动,最终稳定在约8mL的刻度线上。
(5)因为白磷在密闭容器内燃烧产生热量使气体膨胀,可能会使橡胶塞弹出、试管爆裂、不使用弹簧夹可能会使注射器活塞弹出等,造成实验失败。故填:橡胶塞弹出、试管爆裂、注射器活塞弹出等。

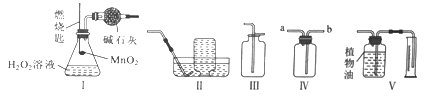
【题目】用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际不相符的是( )

选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钙 | 产生气泡 |
B | 浓硫酸 | 氧化铁 | 产生气泡 |
C | 氯化钡溶液 | 硫酸钾溶液 | 产生白色沉淀 |
D | 氢氧化钠溶液 | 硫酸铜溶液 | 产生蓝色沉淀 |
A. AB. BC. CD. D