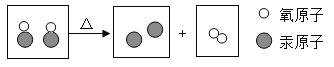
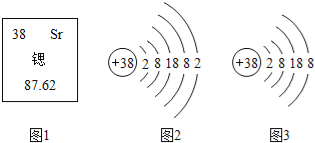
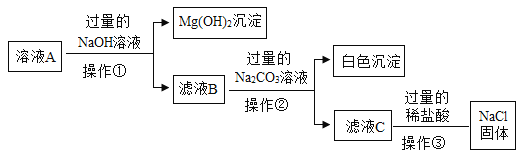
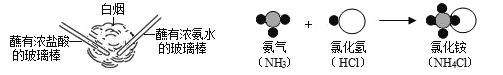
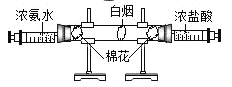
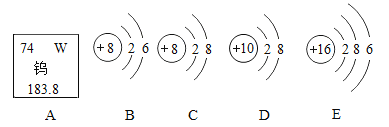题目内容
【题目】用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际不相符的是( )
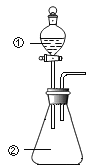
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钙 | 产生气泡 |
B | 浓硫酸 | 氧化铁 | 产生气泡 |
C | 氯化钡溶液 | 硫酸钾溶液 | 产生白色沉淀 |
D | 氢氧化钠溶液 | 硫酸铜溶液 | 产生蓝色沉淀 |
A. AB. BC. CD. D
【答案】B
【解析】
A、稀盐酸和碳酸钙反应生成氯化钙和水和二氧化碳;
B、浓硫酸和氧化铁反应生成硫酸铁和水;
C、氯化钡和硫酸钾反应生成硫酸钡沉淀和氯化钾;
D、硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠。
A、稀盐酸和碳酸钙反应生成氯化钙和水和二氧化碳,有气泡产生,故正确;
B、浓硫酸和氧化铁反应生成硫酸铁和水,没有产生气泡,故错误;
C、氯化钡和硫酸钾反应生成硫酸钡沉淀和氯化钾,有白色沉淀生成,故正确;
D、硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,有蓝色沉淀生成,故正确;故选:B。

【题目】某研究小组受MnO2催化过氧化氢分解的启发,查阅了不同金属离子对过氧化氢分解影响的实验资料。100℃时,在不同金属离子存在下,纯过氧化氢24h的分解率见下表:
实验编号 | 离子 | 加入量(mgL-1) | 分解率% |
① | 无 | - | 2 |
② | Al3+ | 1.0 | 2 |
③ | Fe3+ | 1.0 | 15 |
④ | Cu2+ | 0.1 | 86 |
⑤ | Cr3+ | 0.1 | 96 |
请回答:
(1)MnO2催化过氧化氢分解的化学方程式为______;
(2)实验①的目的是_____________;
(3)实际生产中,贮运浓度较高的过氧化氢时,使用铝罐(槽)而不使用不锈钢罐(槽),其原因是_____。
【题目】2019年5月,187个国家签署了限制塑料废物交易协定,应对“白色污染”挑战。已知某种塑料的组成元素中有碳、氢两种元素,还可能有氧、氯元素中的一种或两种。为了测定其组成,某化学兴趣小组进行如下的探究。
(查阅资料)①无水氯化钙固体可做干燥剂;②有机物中的氯元素燃烧后通常转化为氯化氢。
(设计实验)兴趣小组设计并进行了如图所示的实验。(装置气密性良好)
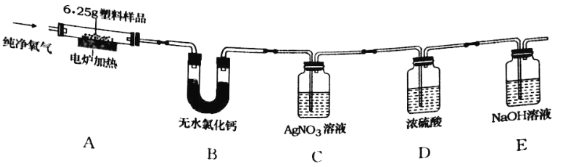
实验过程中,在装置C中观察到________现象,证明该塑料样品中含有氯元素,该反应的化学方程式是________。
(记录数据)6.25g样品在A装置中充分燃烧,反应产物被完全吸收后,测得相关实验数据如表。
装置 | B | C | D | E |
反应后装置增加的质量/g | 1.80 | 3.65 | 0.09 | 8.80 |
(分析与结论)根据以上数据分析与计算,6.25g样品中氢元素的质量为________g,该塑料样品的组成元素是________。
(反思评价)电炉加热前要先通一会儿氧气,目的是________。