题目内容
【题目】在一定条件下,一个密闭容器中发生某反应,测得反应过程中各物质的质量如下表所 示,下列说法错误的是( )

A. 反应后 a 物质的质量为 7g B. 该反应中,d 可能是催化剂
C. b 物质可能是单质 D. b、c 的相对分子质量之比一定是 8:11
【答案】D
【解析】
反应后b质量减少了(10g-2g)=8g,是反应物;c质量增加了(21g-10g)=11g,是生成物;d的质量不变,可能是催化剂,也可能没有参加反应,根据质量守恒定律可知,a是反应物,参加反应的质量为=11g﹣8g=3g。
根据上述分析可知:
A、a是反应物,参加反应的质量为=11g﹣8g=3g,反应后 a 物质的质量=(10g-3g)= 7g,故A正确;
B、d的质量在反应前后不变,可能是催化剂,故B正确;
C、在该反应中,a、b是反应物,c是生成物,该反应是由两种物质生成一种物质的反应,属于化合反应,b物质可能是单质,故C正确;
D、反应中b、c的质量比为=8g:11g=8:11,在化学反应中物质的质量之比,不一定等于物质的相对分子质量之比,所以b、c的相对分子质量之比不一定为8:11,故D错误。故选D。

 智能训练练测考系列答案
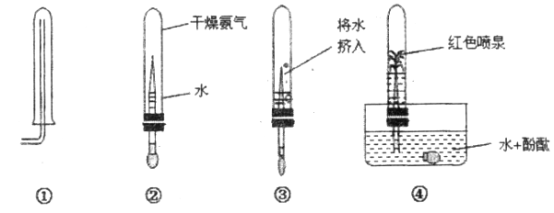
智能训练练测考系列答案【题目】小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧,于是设计了如图所示的装置进行实验探究,请你结合实验过程回答下列问题。
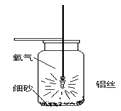
(1)集气瓶底预先铺少量沙子的目的是________。
(2)铝丝下端系一根火柴的目的是:________。
(3)用正确方法引燃铝丝,伸入装有氧气的集气瓶中后,未观察到铝丝发生剧烈燃烧现象,可能的原因是________。
(4)某化学兴趣小组的同学经查阅资料得知:人呼吸中各种气体的体积分数如表所示:
气体 | 吸入气体 | 呼出气体 |
X | 78% | 75% |
Y | 21% | 15% |
二氧化碳 | 0.03% | 3.68% |
水 | 0.02% | 5.44% |
其它 | 0.95% | 0.88% |
①请你判断:表中X是________,Y是________;
②欲证明人呼出的气体中含有水蒸气,其实验方法是___________。
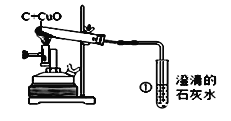
【题目】如图是木炭还原氧化铜的探究实验装置:
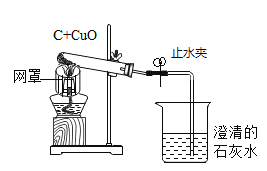
(提出问题)木炭还原氧化铜产生什么气体?
(提出猜想)产生的气体有三种情况:①CO;②CO2;③________。
(设计方案)实验前后分别对试管和烧杯里的物质进行称量,数据设计如下
称量对象 | 反应前质量 | 反应后质量 | 质量差 |
试管+固体混合物 | M1 | M2 | △m1即(M1﹣M2) |
烧杯+澄清石灰水 | M3 | M4 | △m2即(M4﹣M3) |
(1)若△m2=0,说明反应产生的气体不能被澄清石灰水吸收,则猜想_____(填“①”、“②”或“③”)成立。
(2)若猜想②正确,理论上△m1与△m2的关系是:△m1_____△m2(填“>”、“<”或“=”)。
(实验并记录)实验得到的数据如下表:
称量对象 | 反应前质量 | 反应后质量 | 质量差 |
试管+固体混合物 | 69.89g | 65.49g | △m1 |
烧杯+澄清石灰水 | 118.9g | 122.6g | △m2 |
用以上实验数据分析,结果应该是猜想_______(填“①”、“②”或“③”)成立。
同学们对CO产生的原因进行了
原因一:木炭和氧化铜在高温条件下直接发生反应产生CO,反应方程式为:_________。
原因二:木炭和氧化铜在高温条件下反应中的一种产物和反应物木炭又发生了化学反应,产生了CO,反应方程式为:________。
(反思与评价)经查阅资料知道:木炭还原氧化铜产生CO2气体,反应化学方程式为:__________。
本次实验结果与资料显示不一致对其可能原因有同学提出下列分析,其中合理的是_______(填字母)。
A.装置漏气 B.生成的CO2部分与过量的C反应生成了CO
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收
按本装置进行实验,待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是________。
(定量分析)6克碳与一定质量的氧化铜恰好完全反应,生成的气体完全被足量的石灰水吸收,可得到沉淀________克。(要求:写出计算过程)