题目内容
【题目】兴趣小组同学在完成“常见金属的性质"实验时发现了一些异常现象。
(1)将铝片插入硫酸铜溶液中未发现明显的实验现象。请分析出现上述实验现象的原因:____________。为顺利完成实验,建议如何操作?________________。
(2)兴趣小组同学根据建议,重新进行了实验,观察到了明显的实验现象。经充分反应后,该实验的现象是__________________。
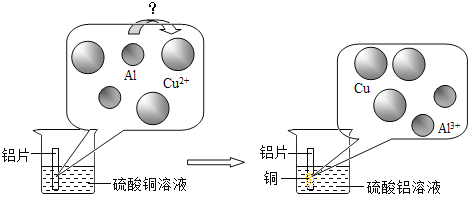
(3)经研究发现该反应的微观示意图如下图所示,图中微粒未完全画出,回答下列问题、
①下列说法中正确的是__________________。
A硫酸铜溶液中含有的微粒是Cu2+、SO42-
B硫酸铜溶液能导电
C反应的实质是Al得电子生成Al3+、Cu2+失电子生成Cu
D硫酸铜溶液呈蓝色,硫酸铝溶液为无色,说明蓝色与Cu2+有关
②反应过程实质是金属铝与硫酸铜溶液中__________(填微粒的化学式)的反应。
(4)在完成上述实验时,有同学发现铝片表面有少量气泡生成。查阅资料得知,硫酸铜在水中会发生一些变化,生成微量的稀硫酸。写出反应中生成气泡的化学方程式______________________。
【答案】铝片表面有一层致密的氧化膜 用砂纸打磨铝片 溶液变成无色,铝片表面有红色固体析出 BD Cu2+ ![]()
【解析】
(1)将铝片插入硫酸铜溶液中未发现明显的实验现象,因为铝片表面有一层致密的氧化铝薄膜,氧化铝与硫酸铜溶液不反应;
为顺利完成实验,应用砂纸打磨铝片,将表面的氧化铝薄膜除去;
(2)铝与硫酸铜反应生成硫酸铝和铜,故实验现象是:溶液变为无色,铝片表面有红色固体析出;
(3)A、硫酸铜溶液中含有的微粒是Cu2+、SO42-、水分子,不符合题意;
B、硫酸铜溶液中含有铜离子和硫酸根离子,能导电,符合题意;
C、反应的实质是Al失去电子生成Al3+、Cu2+得到电子生成Cu,不符合题意;
D、硫酸铜溶液呈蓝色,硫酸铝溶液为无色,它们都含有硫酸根离子,说明蓝色与Cu2+有关,说法正确,符合题意。
故选BD;
②反应过程实质是金属铝与硫酸铜溶液中Cu2+的反应;
(4)铝与稀硫酸反应生成硫酸铝和氢气,该反应的化学方程式为:![]() 。
。

 名校课堂系列答案
名校课堂系列答案【题目】经过监测和治理,我市的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地。某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土壤,并对土壤进行探究。
(查阅资料)①枸杞可在轻度盐碱地中生存。②盐碱地显碱性。③该土样中的可溶性物质只含NaCl、CaCl2和Na2CO3。
(探究过程)(1)甲组探究土壤的酸碱度:具体操作是________________________________________________,由此得出,该土壤的pH>7。
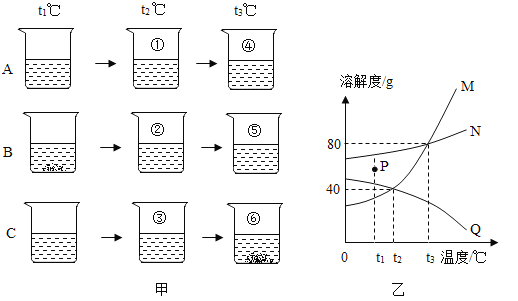
(2)乙组按下图进行实验:向土壤中加入足量的蒸馏水,发生反应的化学方程式为_________________________。该反应属于_____________(填基本反应类型)。

同学们对溶液I中的溶质成分很感兴趣,作出如下猜想:
猜想①:只有氯化钠 猜想②:含有氯化钠、氯化钙 猜想③:含有氯化钠、碳酸钠
设计实验,继续探究:
方案 | 验证猜想所用试剂 | 实验现象 | 实验结果 |
方案一 | AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 猜想① 正确 |
方案二 | 碳酸钠溶液 | ______________ | 猜想② 不正确 |
方案三 | _______________ | 有气泡产生 | 猜想③ 正确 |
(反思与评价)通过交流,甲组认为乙组的方案一不太严谨,理由是_______________。(总结与提升)改良我市的盐碱地,充分利用土地资源,造福百姓,我们任重而道远。以下建议你认为正确的是__________。 (填写字母序号)
a 轻度盐碱地可以种植枸杞
b 可以用熟石灰改良盐碱地
c 盐碱地应避免施用碱性化肥