题目内容
【题目】质量守恒定律的发现对化学的发展做出了很大的贡献。
(1)利用下列各组试剂在密闭容器中进行实验,可以验证质量守恒定律的是_____。
A 蔗糖和水 B 氢氧化钠溶液和硫酸铜溶液 C 白磷和空气
(2)根据微观示意图回答下列问题。在高温条件下,A、B两种物质可以发生化学反应生成C和D.反应前后分子种类变化的微观示意图如下所示。
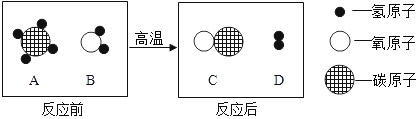
①A,B,C,D四种物质中,属于氧化物的是_____(请用化学式表示)。
②写出该反应的化学方程式______________________________。在该反应中,生成C和D的质量比为_____。
(3)工业上制取氮化硅的化学反应原理是![]() (氮化硅),则氮化硅的化学式为_____。
(氮化硅),则氮化硅的化学式为_____。
【答案】BC H2O和CO 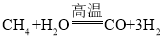 14:3 Si3N4
14:3 Si3N4
【解析】
(1)A. 蔗糖和水是溶解过程,发生物理变化,不能直接用来解释质量守恒定律。故A不符合题意;
B.氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜和硫酸钠,可以验证质量守恒定律。故B符合题意;
C. 白磷和空气在密闭容器中进行实验,反应生成五氧化二磷,也可以验证质量守恒定律。故C符合题意;
故选BC。
(2)根据微观示意图可以知道,该反应是甲烷和水在高温条件下反应生成一氧化碳和氢气的反应,反应的方程式为: 。
。
①氧化物是由氧元素和另一种元素组成的化合物。由方程式可以看出,属于氧化物的物质是一氧化碳和水,化学式为H2O和CO。故填:H2O和CO。
②由以上分析可知反应的方程式为 ,由方程式可得生成C(一氧化碳)和D(氢气)的质量比为28:6=14:3。故填:
,由方程式可得生成C(一氧化碳)和D(氢气)的质量比为28:6=14:3。故填: ;14:3。
;14:3。
(3)由反应的方程式![]() (氮化硅),根据反应前后原子种类个数守恒,可以得出氮化硅的化学式为:Si3N4 。故填:Si3N4。
(氮化硅),根据反应前后原子种类个数守恒,可以得出氮化硅的化学式为:Si3N4 。故填:Si3N4。

【题目】某研究性学习小组以“酸与碱能否发生反应”为课题进行了实验探究。
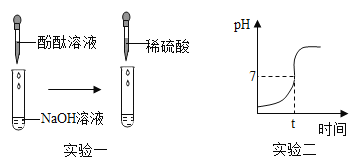
(实验一)
(1)向滴有酚酞试液的NaOH溶液中滴入稀硫酸,观察到溶液颜色由_____,证明硫酸和氢氧化钠发生了反应,该反应的化学方程式为_____。
(2)继续往上述反应后的溶液中逐滴滴入NaOH溶液,不断振荡,如果观察到_____现象,证明了滴加的稀硫酸过量。
(实验二)测量酸和碱反应过程的pH
(1)实验过程中用传感器实时获得溶液的pH,要得到如图所得变化曲线,所进行的操作是_____(填字母)。
A 将稀硫酸溶液逐滴滴加到氢氧化钠溶液中
B 将氢氧化钠溶液逐滴滴加到稀硫酸溶液中
(2)根据如图2溶液pH变化,判断酸和碱发生反应的依据是_____。
(实验三)小组同学经过讨论,一致认为除了上述方法外,还可以按照如表实验方法证明硫酸和氢氧化钠发生了反应。
实验步骤 | 实验现象 | 实验结论 |
取少量氢氧化钠溶液于试管中,加入过量的稀硫酸,再加入少量的氧化铜 | 得到蓝色溶液,无_____ | 氢氧化钠和硫酸发生了化 学反应 |
(拓展延伸)同学们对氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分产生了浓厚的兴趣,于是进行了进一步的探究。
(提出问题)氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分
(提出猜想)猜想一:Na2SO4猜想二:Na2SO4和H2SO4你的合理猜想是:_____。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
取少量反应后的溶液置于试管中_____ | _____ | 猜想二正确 |
(实验反思)在分析化学反应后所得物质成分时,除考虑生成物外还需要考虑反应物是否有剩余。
【题目】化学概念在逻辑上可能存在如图所示关系,对下列概念说法正确的是( )
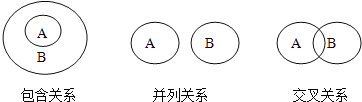
A.纯净物与混合物属于包含关系B.化合反应与氧化反应属于包含关系
C.单质与化合物属于交叉关系D.化合反应与分解反应属于并列关系
【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:相等。
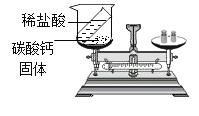
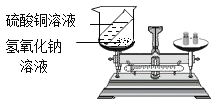
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有_____产生,天平指针向_____偏转 | _____,天平指针没有偏转 |
结论 | 猜想1正确 | 猜想2正确 |
(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在_____中进行。
(改进装置)同学们对甲组左盘中的反应装置进行了如下改进,但是从物理学角度考虑仍有不足,试着指出其不足_____。
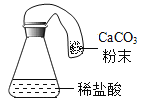
(得出结论)分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论是:_____的各物质的质量总和等于反应后生成的各物质的质量总和。
(微观解释)从微观角度分析,在化学反应前后一定不变的是_____(选填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
【题目】下表列出了20℃时NaCl溶解实验的一组数据
实验序号 | 水的质量/g | 所加NaCl的质量/g | 所得溶液的质量/g |
① | 10 | 2 | 12 |
② | 10 | 3 | 13 |
③ | 10 | 4 | 13.6 |
④ | 10 | 5 | 13.6 |
下列叙述正确的是( )
A.20℃时③所得溶液中NaCl的质量为4 g
B.①所得溶液的溶质的质量分数为20%
C.①②所得溶液是20℃时NaCl的不饱和溶液
D.①②③所得溶液是20℃时NaCl的不饱和溶液