题目内容
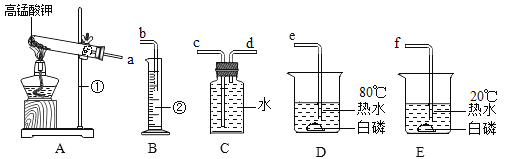
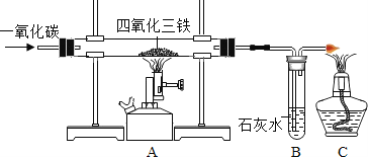
【题目】在实验室里,可以利用如图装置制得铁。
(1)A处玻璃管内所发生反应的化学方程式为______。
(2)B处可观察到的现象是______;C处酒精灯的作用是______
(3)待四氧化三铁完全反应后,停止加热A处,在断开A、B之前应继续通入一氧化碳至A处玻璃管冷却。若不继续通入一氧化碳。可能出现的后果是______。
【答案】澄清的石灰水变浑浊 点燃多余的一氧化碳,避免污染空气 石灰水回流至A处玻璃管中,导致玻璃管炸裂 反应生成的铁被氧化
【解析】
(1)四氧化三铁与一氧化碳在高温条件下生成铁和二氧化碳
(2)二氧化碳能使澄清的石灰水变浑浊,一氧化碳有毒,因此实验过程中未参与反应的一氧化碳要及时处理,防止污染空气,可利用一氧化碳的可燃性进行处理;故答案为:澄清的石灰水变浑浊;点燃多余的一氧化碳,避免污染空气;
(3)停止加热A处,玻璃管温度降低,若不继续通一氧化碳,B处石灰水会回流至A处玻璃管,导致玻璃管炸裂且反应生成的铁被氧化。
故答案为:石灰水回流至A处玻璃管中,导致玻璃管炸裂;反应生成的铁被氧化。
解答本题关键是要知道根据生成物分析实验现象的方法,熟悉方程式的书写方法,知道一氧化碳还原氧化铁的注意事项,尾气的处理方法。

【题目】如图所示,在烧杯A中装有10mL浓氨水,烧杯B中装有20mL蒸馏水,并滴入了几滴酚酞溶液。用一个大烧杯将A、B两个小烧杯罩在一起。一段时间后,B烧杯中的溶液变为红色。关于酚酞变红,化学探究小组同学们提出了三种猜想:( 酚酞溶液是酚酞与水的混合物)
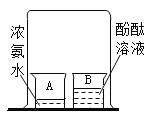
猜想一:从A烧杯中蒸发出水蒸气,部分水分子运动进入B烧杯,使酚酞变红;
猜想二:从A烧杯中挥发出氨气,部分氨分子运动进入B烧杯,使酚酞变红;
猜想三:从A烧杯中挥发出氨气,部分氨分子运动进入B烧杯与水结合形成氨水,使酚酞变红。
(1)同学们经过讨论后一致认为猜想一是不可能的,理由是_____。
(2)为了探究另外两种猜想是否正确,同学们设计了如下实验方案,请填表:
实验操作 | 实验现象 | 实验结论 |
将一张滤纸浸入酚酞溶液中,1min后取出,悬挂在通风处晾干,用剪刀将其剪成两片 | ||
将其中一片干燥滤纸放入收集满氨气的集气瓶中 | 滤纸不变色 | 氨气____(选填“能”或“不能”)使酚酞变红,猜想二___(选填“正确”或“错误”) |
在另一片滤纸上滴几滴蒸馏水,再放入收集满氨气的集气瓶中 | 滤纸变成____色 | 氨气溶解在水中形成氨水,氨水能使酚酞变红,猜想三___(选填“正确”或“错误”) |
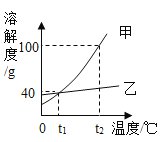
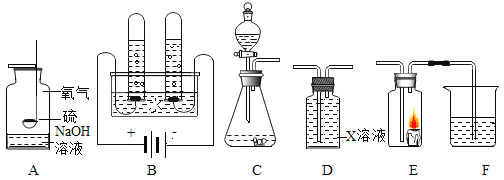
【题目】下列实验操作与图象关系对应正确的是( )
选项 | A | B | C | D |
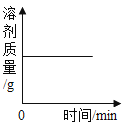
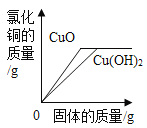
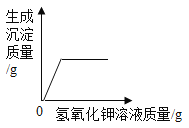
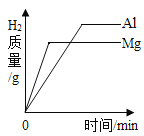
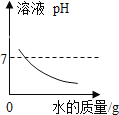
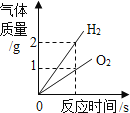
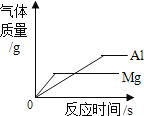
操作 | NaOH溶液中不断加水稀释 | 水电解生成氢气与氧气 | 向等量的稀硫酸中加入足量的镁、铝 | 用等质量、等质量分数的过氧化氢溶液制取氧气 |
图象 |
|
|
|
|
A.AB.BC.CD.D