题目内容
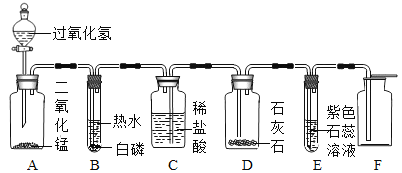
【题目】如图所示为实验室中常见的气体制备、干燥、净化、收集和性质实验的部分仪器,甲、乙两组同学欲用它们完成各自的探究实验。
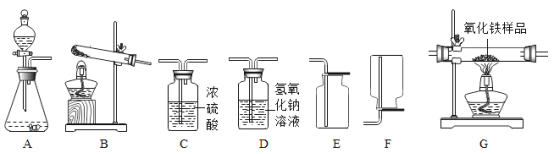
(1)甲组同学以锌粒和稀盐酸为原料制取氢气,因盐酸挥发出少量的氯化氢气体,导致制取的气体不纯,现欲制备并收集一瓶干燥、纯净的氢气,回答下列问题:
①所选仪器的连接顺序为_______。
②反应装置中生成氢气的化学方程式_______。
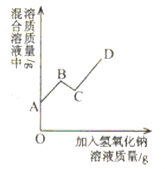
③锌与稀盐酸混合后,随着反应的进行,盐酸溶液的pH将______(填“增大”“减小”“不变”“无法判断”之一)
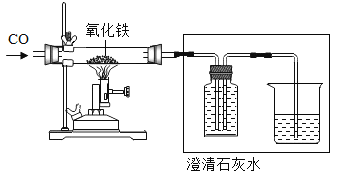
(2)乙组同学欲用水煤气(主要成分为一氧化碳、氢气,含有少量水蒸气)来测定氧化铁样品中Fe2O3的纯度,设计的仪器连接顺序为:水煤气→C1→G→C2→D→C3. (已知:氧化铁样品中的杂质不反应;.![]() ;
; 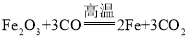 ;其中C1、C2、C3为3个浓硫酸洗气瓶)
;其中C1、C2、C3为3个浓硫酸洗气瓶)
①写出G中的一项实验现象______。
②该同学通过测量反应前后G装置质量的变化,来计算样品中Fe2O3的纯度,若无装置C1,则计算结果会____(填“偏大”“偏小”、“基本一致”之一)。
③实验中该小组学生取用了25g氧化铁样品,经实验测定装置C2增加了2.7g,D装置增加了6.6g,则氧化铁样品的纯度为______。
④从环境保护的角度考虑,该套实验装置存在不足,写出具体改进措施________。
【答案】ADCF ![]() 增大 红棕色粉末变为黑色 偏大 64% C3短导管处套上气球(合理即可)
增大 红棕色粉末变为黑色 偏大 64% C3短导管处套上气球(合理即可)
【解析】
(1)①以锌粒和稀盐酸为原料制取氢气,因盐酸挥发出少量的氯化氢气体,导致制取的气体不纯,通过氢氧化钠溶液将氯化氢除去,然后再通过浓硫酸除去气体中混有的水分,故制备并收集一瓶干燥、纯净的氢气,所选仪器的连接顺序为ADCF,故填:ADCF。
②锌和稀盐酸反应生成氯化锌和氢气,故填:Zn+2HCl═ZnCl2+H2↑。
③锌与稀盐酸混合后,随着反应的进行,盐酸逐渐减少,酸性逐渐减弱,盐酸溶液的pH将增大,故填:增大。
(2)①一氧化碳和氢气具有还原性,能将氧化铁还原为铁,会观察到红棕色粉末变为黑色,故填:红棕色粉末变为黑色。
②该同学通过测量反应前后G装置质量的变化,来计算样品中Fe2O3的纯度,若无装置C1,则水的质量会变大,则计算结果会偏大,故填:偏大。
③实验中该小组学生取用了25g氧化铁样品,经实验测定装置C2增加了2.7g,说明生成水的质量为2.7g,设与氢气反应的氧化铁的质量为x,则有:

x=8g
D装置增加了6.6g,则生成二氧化碳6.6g,设与一氧化碳反应的氧化铁的值为y

y=8g
则氧化铁样品的纯度为:![]() ×100%=64%。
×100%=64%。
故填:64%;
④从环境保护的角度考虑,该套实验装置存在不足,因为一氧化碳是有毒的气体,需要进行尾气处理,故填:C3短导管处套上气球。

 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案【题目】初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣═H2O。如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。

离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
①写出Na2SO4与BaCl2反应的化学方程式: 。
②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成:2Na++SO42﹣+Ba2++2Cl﹣═BaSO4↓+2Na++2Cl﹣。
③删去方程式两边不参加反应的离子:Ba2++SO42﹣═BaSO4↓。
④检查方程式两边各元素的原子个数和电荷总数是否相等。
请回答:
(1)下列各组中的离子,在pH=3的水溶液中能大量共存的是 。
A.Na+、Mg2+、Cl﹣、SO4 2﹣ | B.Na+、K+、Cl﹣、OH﹣ |
C.Na+、Cu2+、Cl﹣、SO42﹣ | D.Na+、K+、Cl﹣、CO32﹣ |
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式 。
(3)写出一个与离子方程式Mg+2H+═Mg2++H2↑相对应的化学方程式 。
(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或 生成,反应就能发生。
【题目】下图是实验室制取气体的常用装置。请回答下列问题。
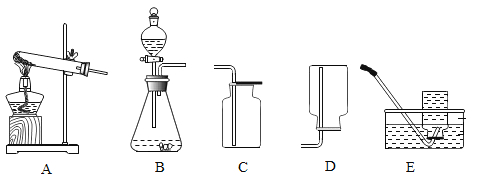
(1)实验室制取气体时,组装好仪器后,应先_____,再添加药品。
(2)实验室选择气体发生装置时,应考虑的因素是_____。
(3)实验室可用上图中的装置来制备和收集一些常见的气体, 请用化学方程式和上图中字母序号填写下表空白。
制取的气体 | 反应原理(用化学方程式表示) | 发生装置 | 收集装置 |
O2 | _____ | A | _____ |
CO2 | _____ | B | D |
(4)通常状况下,甲烷是一种无色无味气体,难溶于水,密度比空气小。实验室常用醋酸钠和碱石灰两种固体混合加热制得,制取并收集甲烷可选用的装置是_____。
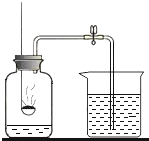
(5)图F是某同学利用报废试管设计的制取二氧化碳的发生装置, 该设计除了废物利用的优点外,请另写一个优点: _____。
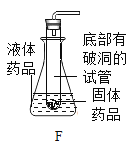
(6)下图是一氧化碳与氧化铁的反应装置中,虚线方框内装置的作用是_____。