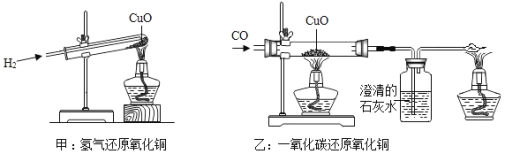
题目内容
【题目】氯化氢(HCl)是极易溶于水的无色气体,其水溶液叫盐酸。

HCl气体 盐酸
(1)在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水,现象是___________________________________________________。
(2)向盛有NaHCO3粉末的试管中通入HCl气体,无明显现象;停止通气,再加入少量水,现象是_____________________,发生反应的化学方程式是___________________。
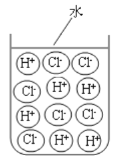
(3)画出HCl气体和盐酸的微观粒子组成示意图,并进行必要的标注_______________(水分子不用画出)。
【答案】染有石蕊的纸条变红色 固体溶解,有气泡产生 ![]()
【解析】
盐酸能使紫色石蕊溶液变红色,碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳。
(1) 酸能使紫色石蕊溶液变红色,在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水,HCl气体溶液水形成盐酸,现象是染有石蕊的纸条变红色。
(2)向盛有NaHCO3粉末的试管中通入HCl气体,无明显现象;停止通气,再加入少量水,HCl气体溶液水形成盐酸,碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,现象是固体溶解,有气泡产生,发生反应的化学方程式是![]() 。
。
(3) HCl气体溶于水形成盐酸,盐酸会电离出氢离子和氯离子,故微观粒子组成示意图为


【题目】某学校化学学习小组对实验室用过氧化氢溶液制O2的知识做了多方位的探究,下面是他们的学习实录:
(1)实验发生装置的探究学习:根据反应物的状态,甲同学从下列装置中选择了C作为发生装置,你认为他该选择的收集装置是_____.
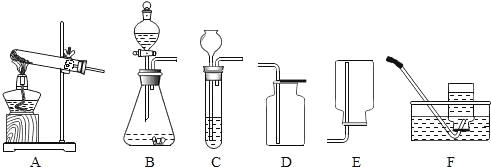
实验过程中甲同学发现,试管中产生了很多泡沫,甚至有些进入导气管中.乙同学将发生装置改成了B,解决了这个问题.你认为理由是_____.
(2)催化剂选择的探究学习:
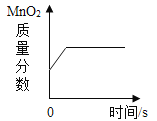
通过课堂上的学习,丙同学了解到:MnO2、土豆块都可以做H2O2分解的催化剂,于是萌生了寻找适合催化剂的想法.通过查阅资料,他还了解到部分盐(溶液)也对过氧化氢的分解具有催化作用,如CuCl2、CuSO4等盐(溶液).于是他做了以下的探究.
①请你帮助他完成实验报告:
实验过程 | 实验现象 | 实验结论 |
在一支试管中加入5mL6%的H2O2溶液,然后滴入适量的CuCl2溶液,把带火星的木条伸入试管. | CuCl2溶液可以催化分解H2O2 |
②已知CuCl2在水中可解离出Cu2+和Cl﹣,同学们提出以下猜想:
丁同学说:真正催化分解H2O2的是CuCl2溶液中的H2O;
戊同学说:真正催化分解H2O2的是CuCl2溶液中的Cu2+;
戌同学说:真正催化分解H2O2的是CuCl2溶液中的Cl﹣;
经过讨论,同学们认为最不可能的是丁同学的猜想,理由是_____.
最后他们通过实验证明了是溶液中的Cu2+对H2O2分解起了催化作用.
【题目】去年,江西省出台了禁止在城区燃放烟花爆竹的规定。针对烟花爆竹燃放产生的气体成分,某校化学小组的同学展开了如下探究
(提出问题)烟花爆竹燃烧后生成哪些气体?
(查阅资料)
①烟花爆竹的主要成分是黑火药,含有硫黄、木炭粉、硝酸钾。
②SO2易溶于水其化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3.将SO2通入紫色的酸性高锰酸钾溶液中,溶液会褪色。
(做出猜想)猜想I:CO2;猜想Ⅱ:______;猜想Ⅲ:CO2和SO2。
(实验探究)化学小组同学合作设计了如图实验装置,验证猜想的气体。
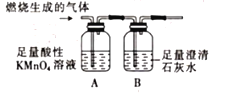
(现象与结论)
现象 | 结论 |
①装置A中溶液不褪色,装置B中 ______ | 猜想I成立 |
②装置A中溶液会褪色,装置B中澄清石灰水变浑浊 | ______ |
③装置A中 ______ ,装置B中 ______ | 猜想Ⅱ成立 |
(反思评价)小组经过讨论后认为A、B装置的顺序不能颠倒。
【题目】实验室配制饱和澄清石灰水和质量分数为10%的氢氧化钠溶液,并进行有关实验。
下表是20℃时部分物质的溶解度数据。
物质 | Ca(OH)2 | NaOH | CaCO3 | Ca(HCO3)2 | Na2CO3 | NaHCO3 |
溶解度/g | 0.16 | 109 | 0.0065 | 16.6 | 21.8 | 9.6 |
(1)配制溶液。其中配制100g10%氢氧化钠溶液的基本步骤是:
称取氢氧化钠固体—量取水—溶解—装瓶贴标签。

①称取氢氧化钠固体的质量_____________g。
②已知水的密度为1g/cm3,用100mL量筒量取所需的水,_______画出水的液面。
③装瓶后贴标签,在标签上填写:_______________________________。
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向饱和澄清石灰水中通入CO2直至过量,先生成CaCO3,再转化为Ca(HCO3)2,可观察到的现象是________________________________。
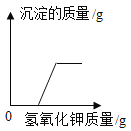
②向10%氢氧化钠溶液中通入CO2直至过量,先生成Na2CO3,再转化为NaHCO3,可观察到的现象是_______________________________________________________。
③理论上吸收4.4gCO2,需饱和澄清石灰水的质量至少为___________g,或需10%氢氧化钠溶液的质量至少为__________g。(计算结果精确到个位)
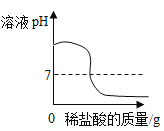
【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_____,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
(实验用品)pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
(猜想与假设)反应后溶液中溶质的可能组成成分。
猜想一:硫酸钠
猜想二:硫酸钠、碳酸氢钠
猜想三:硫酸钠、硫酸
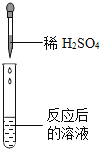
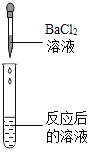
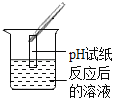
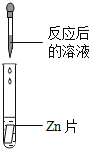
(实验探究)同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成如表实验现象中的空格。
实验方案 | A | B | C | D |
实验操作 |
|
|
|
|
实验现象 | _____ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH<7 | _____ |
实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
(得出结论)猜想三正确。
(评价反思)
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显的操作错误是_____。
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由_____。
(总结提高)依据所给实验用品,设计与上述实验不同的方案,确认猜想三是正确的,请你写出你的实验方案_____。