题目内容
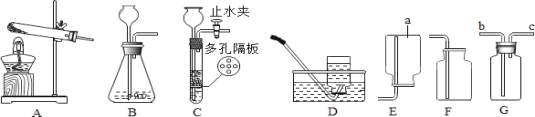
【题目】老师用如图所示装置为同学们做了一个兴趣实验。已知装置B、C、D中依次盛有紫色石蕊溶液,足量的澄清石灰水和稀盐酸。
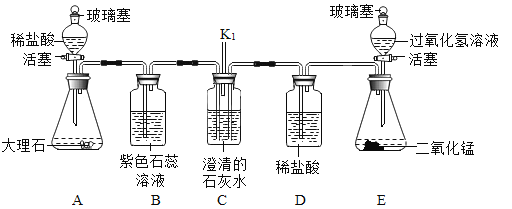
(1)写出标号的仪器名称:a_____;b_____。
(2)打开A中的玻璃塞和活塞,待反应进行一段时间后,可以看到B中的紫色石蕊溶液_____,C中的澄清石灰水变浑浊。
(3)关闭A中的活塞和玻璃塞,打开E中的玻璃塞和活塞,待足量的过氧化氢溶液进入锥形瓶后,关闭E中的活塞,E中反应的化学方程式为_____。反应一段时间后,观察到D中液体沿着导管逐渐流向C中,此时C中可能出现的现象是_____。写出此时C中发生反应的化学方程式_____。
(4)上述实验过程中,C中玻璃管K1的作用是_____。
【答案】锥形瓶 导管 变红色 2H2O2![]() 2H2O+O2↑ 液面上升,白色固体逐渐溶解,有无色气泡产生 CaCO3+2HCl=CaCl2+H2O+CO2↑ 排出生成的气体,避免装置中压强过大
2H2O+O2↑ 液面上升,白色固体逐渐溶解,有无色气泡产生 CaCO3+2HCl=CaCl2+H2O+CO2↑ 排出生成的气体,避免装置中压强过大
【解析】
(1)由图可知,仪器a是锥形瓶,故填锥形瓶;
仪器b是导管,故填导管。
(2)大理石与稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色,故填变红色。
(3)E中的反应是过氧化氢在二氧化锰的催化作用下分解为水和氧气,故反应的化学方程式写为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
由于E中氧气放出,使D中压强增大,D中的稀盐酸流入C,则稀盐酸与C中沉淀(A中反应生成的二氧化碳和C中石灰水反应生成的碳酸钙)反应,生成二氧化碳气体,所以观察反应现象为:液面上升,白色固体逐渐溶解,有无色气泡产生,故填液面上升,白色固体逐渐溶解,有无色气泡产生;
稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,故反应的反应方程式写为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
(4)因A,E中都产生气体,C中玻璃管K1的作用是排出装置中气体,减小压强,故填排出生成的气体,避免装置中压强过大。

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案