题目内容
【题目】工业上采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)来制取绿矾(FeSO4·7H2O),实现变废为宝,减少环境污染。简易流程如下: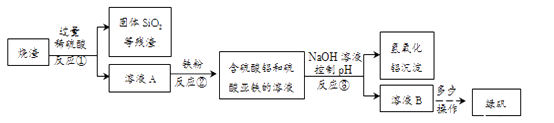
(1)反应①和反应③都要进行的操作是;
(2)写出反应②中发生反应的化学方程式为;
(3)用NaOH溶液控制pH的目的是。
【答案】
(1)过滤
(2)Fe+H2SO4=FeSO4+H2↑、 Fe+ Fe2(SO4)3=3FeSO4
(3)使Al3+完全转化为Al(OH)3沉淀
【解析】(1)反应①和反应③要进行过滤操作;
(2)反应的化学方程式为Fe+H2SO4=FeSO4+H2↑和Fe+Fe2(SO4)3=3FeSO4;
(3)要通过加入氢氧化钠溶液控制溶液的pH来实现只让铝离子沉淀,而不让亚铁离子沉淀。(1)反应①和反应③后都是生成难溶性物质(残渣或沉淀)和溶液,要将两者分离开来,必须使用过滤操作来达到实验目的;(2)由于反应①加入的硫酸是过量的,且和矿石反应生成了硫酸铝和硫酸铁,铁能够和剩余的硫酸生成硫酸亚铁和氢气,以及和硫酸铁反应生成硫酸亚铁。所以反应②中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑和Fe+Fe2(SO4)3=3FeSO4;(3)由于溶液中既有亚铁离子也有铝离子,这两者遇到氢氧根离子都会反应生成沉淀,所以要通过加入氢氧化钠溶液液控制溶液的pH来实现只让铝离子全部转化为氢氧化铝沉淀,而不让亚铁离子沉淀。

练习册系列答案
相关题目