题目内容
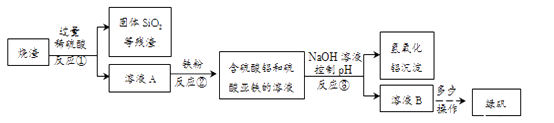
【题目】硅(Si)是信息技术的关键材料,以石英砂(主要成分为SiO2)为原料制得纯硅的生产过程如下图所示: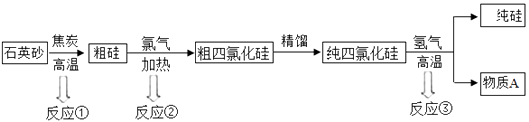
(1)反应①中会排放出CO,CO极易与血液中的结合,从而使其不能再与氧气结合,造成生物体缺氧。
(2)反应②对应的化学方程式为。
(3)反应③所属基本反应类型为;物质A的水溶液可用来除铁锈,发生反应的化学方程式为。
(4)100 t含SiO2 90%的石英砂,理论上可生产纯硅的质量是。
【答案】
(1)血红蛋白
(2)Si+2Cl2 ![]() SiCl4
SiCl4
(3)置换反应,Fe2O3+6HCl=2FeCl3+3H2O
(4)42t
【解析】解:(1)CO有巨毒,反应①中会排放出CO,CO极易与血液中的血红蛋白结合,从而使其不能再与氧气结合,造成生物体缺氧;(2)反应物是硅和氯气,生成物是四氯化硅,反应条件是加热,故反应②对应的化学方程式为Si+2Cl2![]() SiCl4;(3)反应③是氢气与四氯化硅反应生成硅和盐酸(A),故反应类型是置换反应;物质A的水溶液可用来除铁锈,发生反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O;(4)设理论上可生产纯硅的质量是x。
SiCl4;(3)反应③是氢气与四氯化硅反应生成硅和盐酸(A),故反应类型是置换反应;物质A的水溶液可用来除铁锈,发生反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O;(4)设理论上可生产纯硅的质量是x。
根据题意有下列关系式:
SiO2 — Si — SiCl4 — | Si(纯) |
60 | 28 |
100t×90% | x |
![]()
x=42t
答:理论上可生产纯硅的质量是42t。
所以答案是:血红蛋白、Si+2Cl2![]() SiCl4、置换反应、Fe2O3+6HCl=2FeCl3+3H2O、42t。
SiCl4、置换反应、Fe2O3+6HCl=2FeCl3+3H2O、42t。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】下列实验中,现象与结论对应关系正确的是( )
A | B | C | D | |
图 |
|
|
|
|
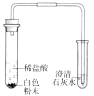
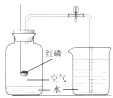
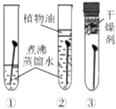
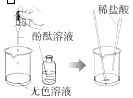
现 | 有大量气泡产生,生成的气体使澄清石灰水变浑浊 | 冷却后,打开弹簧夹,水被吸入瓶内,瓶内水面上升约 1/5 | ①中铁钉生锈, ②③中铁钉不生锈 | 滴加无色酚酞, 溶液呈红色,加入稀盐酸后红色变为无色 |
结论 | 该粉末中一定含有 | 氧气约占空气质量的1/5 | ①②对比说明铁生锈条件之一是要与水接触 | 反应后的溶液一定不呈 |
A.A
B.B
C.C
D.D