题目内容
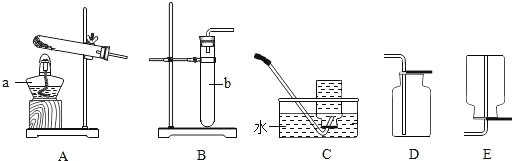
【题目】如图是实验室制取和收集气体的常见装置,回答下列问题:
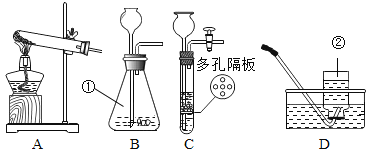
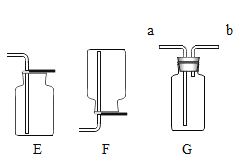
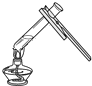
(1)装置中仪器标号①的名称是_____。
(2)实验室利用C、E组合,可以制取_____气体;写出其实验室制取的化学方程式_____。装置C与B相比优点是_____。
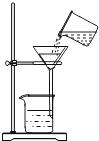
(3)实验室加热氯酸钾制取较纯净的氧气,化学方程式是_____,选用的发生和收集装置是_____(填序号)。用你所选的收集装置收集到的氧气不纯的原因可能是(填出一条即可)_____。
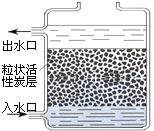
(4)G装置具有广泛的用途。若用其干燥氧气,则气体需要从装置G的_____端进入。
【答案】锥形瓶 二氧化碳 CaCO3+2HCl=CaCl2+H2O+CO2↑ 能随时控制反应的发生与停止 2KClO3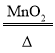 2KCl+3O2↑ AD 集气瓶未灌满水或未等气泡连续均匀的放出就开始收集 a
2KCl+3O2↑ AD 集气瓶未灌满水或未等气泡连续均匀的放出就开始收集 a
【解析】
I、装置中仪器标号①的名称分别是锥形瓶;
Ⅱ、C装置属于固、液常温型发生装置,E装置是向上排空气法收集气体的杂质,所以C、E可以制取二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;装置C与B相比优点是:能够控制反应的发生与停止,反应后关闭开关时,试管中的气体增多,压强增大,固液分离反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,固液接触反应进行;
Ⅲ、氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,反应的化学方程式为:2KClO3![]() 2KCl+3O2↑;利用氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,属于固、固加热型,适合用装置A作发生装置,氧气的密度比空气大,不易溶于水,可用装置D或E或G收集;但要求是较纯净的氧气,故只能选D。排水法收集的气体不纯的主要原因是:集气瓶未灌满水或未等气泡连续均匀的放出就开始收集。
2KCl+3O2↑;利用氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,属于固、固加热型,适合用装置A作发生装置,氧气的密度比空气大,不易溶于水,可用装置D或E或G收集;但要求是较纯净的氧气,故只能选D。排水法收集的气体不纯的主要原因是:集气瓶未灌满水或未等气泡连续均匀的放出就开始收集。
IV、氧气不与浓硫酸反应,而浓硫酸可以吸收水蒸气,所以是长进短出,从a端进入气体。

 学习实践园地系列答案
学习实践园地系列答案【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 2.2 | 6.4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 3.6 | 2.2 | a |
下列判断正确的是( )
A. 表中a的值为2.8 B. X可能是该反应的催化剂
C. X不可能含有氢元素 D. X只含碳元素