题目内容
把7克含杂质的锌片(杂质不与盐酸反应)投入100克足量的稀盐酸里,反应停止后所得混合物的总质量为106.8克。计算:
(1)反应后生成氢气的质量;
(2)不纯的锌片中单质锌的质量分数。(计算结果精确到0.1%)
(1)反应后生成氢气的质量;
(2)不纯的锌片中单质锌的质量分数。(计算结果精确到0.1%)
解析: 根据质量守恒定律,生成氢气的质量为: 7克+100克-106.8克=0.2克
设纯锌的质量为x
Zn + 2HCl === ZnCl2 + H2↑
65 2
x 0.2克

不纯的锌片中单质锌的质量分数为: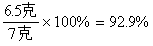
答:生成氢气的质量是0.2克,锌片中锌的质量分数是92.9%。
设纯锌的质量为x
Zn + 2HCl === ZnCl2 + H2↑
65 2
x 0.2克

不纯的锌片中单质锌的质量分数为:
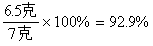
答:生成氢气的质量是0.2克,锌片中锌的质量分数是92.9%。

练习册系列答案
相关题目