题目内容
【题目】锌粒投入硫酸铜溶液中,除了有红色固体生成外,还有一种无色无味的气体产生。为确定气体的成分,进行下列实验探究。
(猜想与假设):依据____可知气体可能是SO2、O2、H2中的一种或几种。
(查阅资料):
①SO2能使酸性高锰酸钾溶液褪色。
②O2+4KI+4HCl=2I2+4KCl+2H2O,淀粉遇I2变蓝。
③H2、CO等气体能将氧化铜还原成铜。
(实验验证):
(1)将气体通入酸性高锰酸钾溶液中,无现象,则该气体中无SO2。小明同学认为没有必要做这个实验,只要根据“无色无味的气体”就可推导出该气体一定不是SO2,他的依据是______。
(2)用下列所示实验检验氢气和氧气:
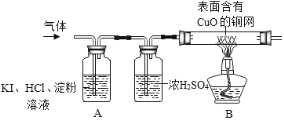
A中观察到 _____,证明无O2;B中观察到 ____,证明该气体是H2。
(实验反思):(1)大家认为丙同学在加热之前,应对气体先_____________以确保安全。
(2)由上述实验可知,硫酸铜溶液显 ______性(填“酸”或“碱”或“中”)。
【答案】质量守恒定律 二氧化硫有刺激性气味 溶液不变色 铜网由黑色变红色,玻璃管壁有水珠生成 验纯 酸
【解析】
解:[猜想与假设]依据质量守恒定律可知气体可能是SO2、O2、H2中的一种或几种;
[实验验证](1)他的依据是二氧化硫有刺激性气味;
(2)A、中观察到溶液不变色,证明无O2;
B、中观察到铜网由黑色变红色,玻璃管壁有水珠生成,证明该气体是H2;
[实验反思](1)大家认为丙同学在加热之前,应对气体先验纯以确保安全,这是因为氢气是可燃性气体,与空气或氧气混合达到一定程度时遇明火或加热会发生爆炸;
(2)由上述实验可知,铁和硫酸铜溶液反应时产生氢气,说明硫酸铜溶液显酸性。

练习册系列答案
相关题目