题目内容
【题目】小青在实验室发现一瓶长期敞口放置的浓盐酸,为方便以后使用,他对其浓度进行了测定.取10g该盐酸于烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)测定溶液的pH,得到的数据如下:
加入氢氧化钠的体积/mL | 0 | 1.0 | 8.0 | 9.5 | 10.5 | 12.0 | 16.5 |
烧杯中溶液的pH | 1.0 | 1.3 | 2.0 | 3.9 | 9.9 | 11.9 | 12.8 |
(1)请你绘制出烧杯中溶液的pH与加入氢氧化钠溶液体积(V)之间的变化关系图.
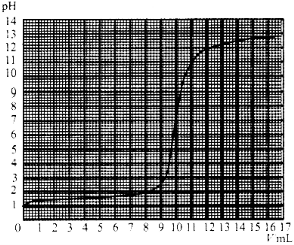
(2)请根据下图找出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积数,并据此计算该瓶盐酸的溶质质量分数.(氢氧化钠溶液的密度按1.0g/mL计算)
【答案】(1)
(2)3.65%
【解析】(1)在描绘曲线图时,要注意几个特别的点:起点和两个拐点(氢氧化钠的体积分别为8.0mL和10.5mL时),这两个拐点决定了曲线的变化趋势,拐点描绘要平滑圆润.
(2)当氢氧化钠与盐酸恰好完全反应时,溶液的pH应为7.0,从曲线土找出此时消耗氢氧化钠的体积约为10.0mL,根据化学方程式中NaOH与HCl的质量比,即可求得HCl的质量分数.
(2)解:由上图可知,恰好完全反应时消耗氢氧化钠溶液的体积约为10.0mL(9.7~10.3mL之间取值均可).
参加反应的NaOH的质量为:
10.0mL×1.00g/mL×4%=0.4g
设盐酸的质量分数为x.
HCl+NaOH=NaCl+H2O
36.5 40
10gx 0.4g
![]()
x=0.0365=3.65%
答:此瓶盐酸的溶质质量分数是3.65%.

练习册系列答案
相关题目