题目内容
【题目】下表是NaCl、KClO3在不同温度下的溶解度(单位:g/100g水).
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
S(NaCl) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
S(KClO3) | 3.3 | 7.3 | 13.9 | 23.8 | 37.5 | 56.3 |
(1)20℃时,NaCl的溶解度为;40℃时,将20g KClO3放入100g水中,所得溶液溶质质量分数为(精确到0.1%).
(2)“海水晒盐”利用的方法是(填“蒸发结晶”或“降温结晶”);
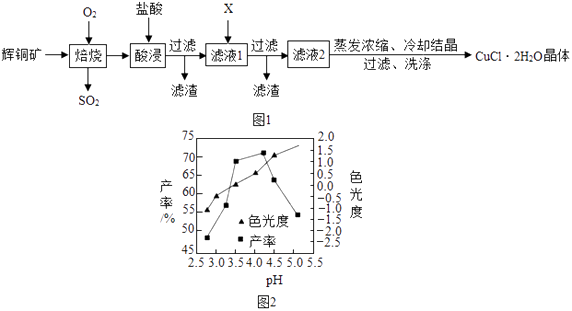
(3)工业上用氯化钠溶液制备氯酸钾,主要流程如下: 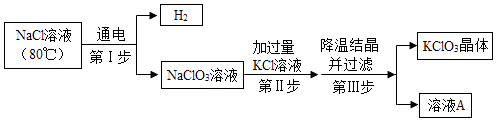
①上述流程中,氯化钠溶液中的水是否参与第I步化学反应?(填“是”或“否”),你的判断依据是 .
②写出第III步中发生反应的化学方程式 .
③溶液A中的溶质除NaCl外,还含有(填化学式).
【答案】
(1)36.0g;12.2%
(2)蒸发结晶
(3)是;元素守恒;NaClO3+KCl=NaCl+KClO3;KCl、KClO3
【解析】解:(1)由表格中数据可知,20℃时,NaCl的溶解度为 36.0g;40℃时,将20g KClO3放入100g水中,由于40℃时,KClO3的溶解度为13.9g,所以只能溶解其中的13.9g,所得溶液溶质质量分数为 ![]() ×100%≈12.2%.(2)由于氯化钠的溶解度受温度影响较小,所以“海水晒盐”利用的方法是 蒸发结晶;(3)①上述流程中,由于第一步生成物是NaClO3和氢气,根据质量守恒定律中的元素守恒可知,水应该是参与了该反应,生成了氢气等.②第III步中,是NaClO3和氯化钾生成了KClO3和氯化钠,该反应的发生是因为KClO3在该温度变化过程中溶解度变化最大而析出,对应的化学方程式 NaClO3+KCl=NaCl+KClO3 . ③由于反应中加入了过量的氯化钾,且反应生成了氯化钠,同时得到KClO3晶体,由于晶体析出后剩余溶液依旧是该物质的饱和溶液,所以体溶液A中的溶质除NaCl外,还含有 KCl、KClO3(填化学式).所以答案是:(1)36.0g;12.2%;(2)蒸发结晶;(3)①是;元素守恒;②NaClO3+KCl=NaCl+KClO3;③KCl、KClO3 .
×100%≈12.2%.(2)由于氯化钠的溶解度受温度影响较小,所以“海水晒盐”利用的方法是 蒸发结晶;(3)①上述流程中,由于第一步生成物是NaClO3和氢气,根据质量守恒定律中的元素守恒可知,水应该是参与了该反应,生成了氢气等.②第III步中,是NaClO3和氯化钾生成了KClO3和氯化钠,该反应的发生是因为KClO3在该温度变化过程中溶解度变化最大而析出,对应的化学方程式 NaClO3+KCl=NaCl+KClO3 . ③由于反应中加入了过量的氯化钾,且反应生成了氯化钠,同时得到KClO3晶体,由于晶体析出后剩余溶液依旧是该物质的饱和溶液,所以体溶液A中的溶质除NaCl外,还含有 KCl、KClO3(填化学式).所以答案是:(1)36.0g;12.2%;(2)蒸发结晶;(3)①是;元素守恒;②NaClO3+KCl=NaCl+KClO3;③KCl、KClO3 .
【考点精析】关于本题考查的结晶的原理、方法及其应用和书写化学方程式、文字表达式、电离方程式,需要了解结晶的两种方法:蒸发溶剂,如NaCl(海水晒盐)和降低温度(冷却热的饱和溶液,如KNO3);注意:a、配平 b、条件 c、箭号才能得出正确答案.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案