题目内容
【题目】下列实验方法不能达到实验目的是( )
A.除去粗盐中的难溶性杂质﹣﹣将粗盐溶解、过滤、蒸发
B.除去CO中的CO2﹣﹣﹣通入足量的氢氧化钠溶液
C.除去热水瓶胆中的水垢﹣﹣用食醋
D.鉴别稀盐酸、氢氧化钠溶液、氯化钠溶液﹣﹣滴加无色酚酞溶液
【答案】D
【解析】解:A、粗盐经过溶解、过滤、蒸发可以得到精盐,故A正确;B、二氧化碳会与氢氧化钠反应,所以除去CO中的CO2﹣﹣﹣通入足量的氢氧化钠溶液,故B正确;
C、热水瓶胆中水垢的主要成分是碳酸钙,碳酸钙会与盐酸反应生成氯化钙、水和二氧化碳,故C正确;
D、无色酚酞在酸性、中性溶液中都不会变色,所以无色酚酞不能鉴别稀盐酸和氯化钠溶液,故D错误.
故选:D.

 阅读快车系列答案
阅读快车系列答案【题目】下表是NaCl、KClO3在不同温度下的溶解度(单位:g/100g水).
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
S(NaCl) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
S(KClO3) | 3.3 | 7.3 | 13.9 | 23.8 | 37.5 | 56.3 |
(1)20℃时,NaCl的溶解度为;40℃时,将20g KClO3放入100g水中,所得溶液溶质质量分数为(精确到0.1%).
(2)“海水晒盐”利用的方法是(填“蒸发结晶”或“降温结晶”);
(3)工业上用氯化钠溶液制备氯酸钾,主要流程如下: 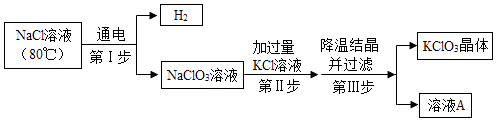
①上述流程中,氯化钠溶液中的水是否参与第I步化学反应?(填“是”或“否”),你的判断依据是 .
②写出第III步中发生反应的化学方程式 .
③溶液A中的溶质除NaCl外,还含有(填化学式).
【题目】“侯氏制碱法”首先得到的碳酸氢钠,然后将碳酸氢钠加热分解得到产品碳酸钠,反应的化学方程式为: 2NaHCO3 ![]() Na2CO3+CO2↑+H2O.碳酸钠置露在空气中能与空气中的二氧化碳和水反应生成碳酸氢钠:Na2CO3+CO2+H2O═2NaHCO3 . 某中学化学学习小组对一瓶开启后久置的碳酸钠是否变质及变质程度进行探究.
Na2CO3+CO2↑+H2O.碳酸钠置露在空气中能与空气中的二氧化碳和水反应生成碳酸氢钠:Na2CO3+CO2+H2O═2NaHCO3 . 某中学化学学习小组对一瓶开启后久置的碳酸钠是否变质及变质程度进行探究.
【提出问题】假设Ⅰ:完全变质;假设Ⅱ:没有变质;假设Ⅲ:部分变质.
【查阅资料】碳酸氢钠溶液不与CaCl2溶液反应
【实验探究】
实验步骤 | 实验现象 | 实验结论 |
取少量样品于试管中,加水溶解后再加入少量CaCl2溶液 | 产生白色沉淀 | 假设不成立,反应的化学方程式为 . |
取少量样品于试管中,用导管连接后固定在铁架台上,导管的另一端插入澄清石灰水中.加热样品 | 有气体产生,澄清的石灰水变浑浊 | 假设不成立.则样品的成分是 . |
【交流反思】欲除去Na2CO3变质后的杂质,最合适的方法是 .