题目内容
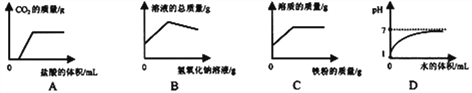
【题目】下列4个图像能正确反映对应变化关系是
A | B | C | D |
|
|
|
|
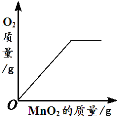
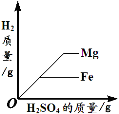
向盛有一定量的H2O2溶液的烧杯中加入MnO2 | 向盛有一定量碳酸钙粉末的烧杯中加入稀盐酸 | 向等质量的镁、铁两种金属,分别放入同浓度的稀硫酸 | 引燃密闭集气瓶中的木炭 |
【答案】A
【解析】
试题分析:向盛有一定量的H2O2溶液的烧杯中加入MnO2 ,但过氧化氢完全分解后氧气的质量保持不变,A正确;向盛有一定量碳酸钙粉末的烧杯中加入稀盐酸会生成氯化钙、水和二氧化碳,由于水中含有氧元素,故烧杯中氧元素的质量不会为零,B错误;向等质量的镁、铁两种金属,分别放入同浓度的稀硫酸,因为没有指明硫酸的质量故不能确定生成氢气的质量关系,C错误;引燃密闭集气瓶中的木炭,氧气的质量一定,当氧气完全消耗好,木炭不能继续燃烧,二氧化碳的质量不变,D错误。故选A。

【题目】根据提供的实验装置回答问题.
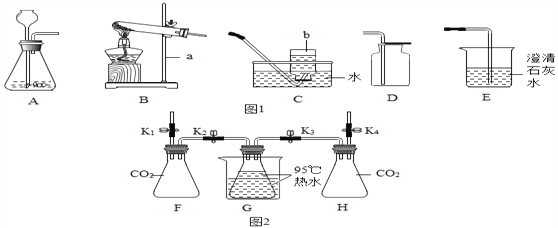
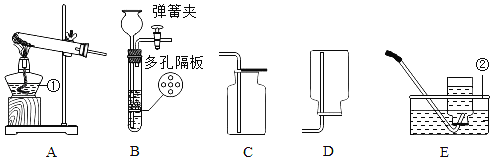
(1)写出仪器名称:a为_____;b为_____
(2)实验室用B装置做高锰酸钾制取O2的发生装置应做何改进_______,发生反应的化学方程式为_______________.
(3)实验室制取CO2的发生和收集装置是_____(填字母序号),CO2通过E装置可观察到的实验现象是_____.小明在实验中用C装置收集到一瓶CO2,为了弄清其中道理,他采取的科学态度和方法是_____(填数字序号).
①置之不理 ②查阅资料 ③交流讨论 ④请教老师
(4)CO2能与NaOH发生反应.
[实验过程]检查装置气密性,如图2所示连接好装置,进行实验.
序号 | 操作步骤 | 实验现象 |
Ⅰ | 打开弹簧夹K1,关闭弹簧夹K2、K3、K4.将20mL水注入锥形瓶F中,关闭弹簧夹K1,振荡瓶G,打开弹簧夹K2 | 无明显现象 |
Ⅱ | 关闭弹簧夹K2,打开弹簧夹K4,将20mL NaOH溶液注入锥形瓶H中,关闭弹簧夹K4,振荡瓶H,打开弹簧夹K1 | 锥形瓶G中的热水剧烈沸腾 |
[实验分析]锥形瓶G中热水剧烈沸腾的原因是_____.
[实验反思]有观点认为只需要进行实验操作Ⅱ,即可说明CO2与NaOH发生反应.你对该观点的看法是_____(选填“赞同”或“不赞同”),理由是_____.
【题目】锌及其氧化物(ZnO,白色,难溶于水,溶于强酸)具有广泛的应用。
(一)锌的广泛应用
(1)锌被称之为“生命元素”。儿童、青少年如果缺锌严重,将会导致“____ 症”和智力发育不良。经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”。这里的“锌”是指__________。
A.单质 B.元素 C.原子 D.分子
(2)实验室用锌与稀硫酸制取氢气,反应的化学方程式为__________________________。
(3)锌与铜熔合可形成“黄铜”,它属于______(选填序号)。
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
(二)活性ZnO制取的探究
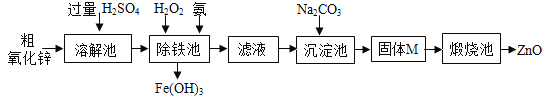
【实验方案】工业上用粗氧化锌(含少量FeO)制取活性氧化锌,其流程如下:
【查阅资料】一些阳离子以氢氧化物形式开始沉淀、完全沉淀时溶液的pH见下表。
沉淀物 | Fe(OH)3 | Zn(OH)2 | Fe(OH)2 |
开始沉淀pH | 1.5 | 6.2 | 6.3 |
完全沉淀pH | 3.2 | 8.0 | 9.7 |
【问题探究】
(4)“溶解”前将粗氧化锌粉碎成细颗粒,目的是___________________。
(5)“溶解”后得到的酸性溶液中含有ZnSO4、____、FeSO4。除铁池中加入适量H2O2,使Fe2+转化为Fe3+;为使溶液中Fe3+全部转化为Fe(OH)3,而Zn2+不形成Zn(OH)2,则应加入氨水控制溶液的pH的范围为_____________。
(6)“沉淀池”中的沉淀经过滤、洗涤等操作得纯净固体M,其组成为:aZnCO3·bZn(OH)2·cH2O。
确认固体M已经洗涤干净的操作是:取最后一次洗涤液,最好选择下列_______,向其中滴入无现象,则已经洗干净。
A.紫色石蕊试液 B.少量稀盐酸 C.氯化钡溶液或硝酸钡溶液
【组成测定】固体B的组成会影响制得的ZnO的活性。为确定aZnCO3·bZn(OH)2·cH2O的组成,进行如下实验(假设每步反应、吸收均完全):
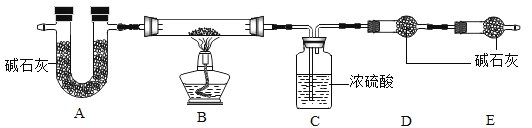
【查阅资料】aZnCO3·bZn(OH)2·cH2O受热分解生成ZnO、H2O、CO2三种产物。
(7)写出装置B中发生反应的化学方程式______________________。
现称取35.9 g aZnCO3·bZn(OH)2·cH2O在B装置中进行完全煅烧,测得装置C和D的质量分别增重7.2 g和4.4 g。
【实验分析及数据处理】
(8)该实验反应前后均需要通入空气,反应后通入空气的目的是_______。
(9)装置A的作用是__________________。
(10)根据上述数据,则生成ZnO的质量为______g;a:b:c=________。
(11)若没有E装置,则测得的a值________(填“偏大”、“ 偏小”或“不变”)。
【题目】有关金属的性质。
I. 把一定质量的锌粉投入到硫酸亚铁和硫酸铜的混合溶液A中,充分搅拌,过滤。回答下列问题。
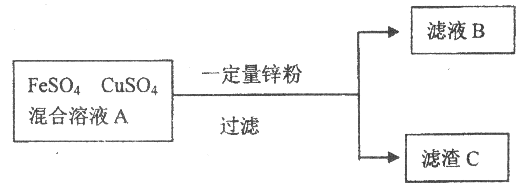
(1)若向滤渣C中加入适量稀硫酸,有气体生成。滤渣C中一定有____________,滤液B中除水外,一定有___________。
(2)若向溶液A中加入过量的锌粉,写出向滤渣C中加入足量硫酸,发生的反应的化学方程式为__________________。
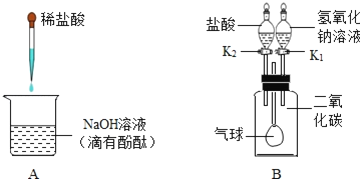
II. 为了验证金属活动性强弱和验证质量守恒定律,同学们设计了如图所示的实验。
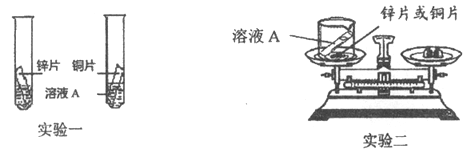
(1)利用实验一和实验二,既能验证铜、锌金属活动性强弱,同时能验证质量守恒定律,则溶液A可以是_________(填序号)。
a. 稀硫酸 b. 硝酸银溶液 c. 氯化亚铁溶液 d. 硫酸锌溶液 e. 硫酸铜溶液
(2)利用以上试剂设计反应,验证铜和银的金属活动性,化学反应方程式为_________,现象为_________。
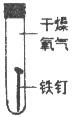
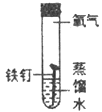
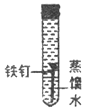
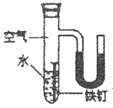
III. 某同学为了探究铁钉生锈条件,设计了如下实验。
序号 | ① | ② | ③ | ④ |
实验内容 |
|
|
|
|
实验现象 | 铁钉无明显变化 | 铁钉生锈 | 铁钉无明显变化 | 铁钉生锈 |
(1)通过实验①、②对比得出的结论是_________。
(2)实验④中,一段时间后,观察到U型管左侧液面_________(填“上升”、“不变”或“下降”),原因是_________。