题目内容
【题目】在反应2A+5B═2C+4D中,C﹑D的相对分子质量之比为9:22,若2.6g A与B完全反应后,生成8.8g D.则在此反应中B与D的质量比为( )
A. 4:9B. 8:1C. 10:11D. 31:44
【答案】C
【解析】
根据C、D的相对质量之比及反应中C、D物质的分子个数关系,计算出参加反应中两物质的质量关系;根据C、D物质的质量关系,由生成D的质量计算出生成C物质的质量;最后使用质量守恒定律,求得参加反应的B物质的质量,即可计算出B与D的质量比.
根据“C、D相对分子质量之比为9:22”,则假设C、D相对分子质量分别为9、22,
设生成8.8gD同时生成C的质量为x,
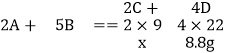
![]()
![]()
根据质量守恒定律参加反应的B的质量为1.8g+8.8g﹣2.6g=8g,则B与D的质量比为8g:8.8g=10:11。
故选C

练习册系列答案
相关题目
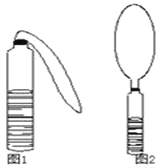
【题目】(1)小杰在一个玻璃瓶中装了半瓶液体,从另一个玻璃瓶中用镊子取出了一些固体颗粒,他把固体的小颗粒用镊子投入瓶中,立即将瘪气球的开口端套住瓶口,再用橡皮筋拉紧,如图1所示,不久,大家看到气球膨胀起来了,如图2,要产生这种现象,则可能的物质组合是:
液体 | 固体 | |
可能1 | _____ | _____ |
可能2 | _____ | _____ |
(2)小明在塑料瓶里装了液体后,充入了一种气体,立即拧紧瓶盖,一会儿,瓶子变瘪了,如图2,要产生这种现象,则可能的物质组合是:
液体 | 固体 | |
可能1 | _____ | _____ |
可能2 | _____ | _____ |