题目内容
赤铁矿(主要成分是Fe2O3)是冶炼生铁的主要原料.若测得某赤铁矿石中铁元素的质量分数为56%.(假设杂质不含铁元素)请回答下列问题:(1)氧化铁中铁元素与氧元素的质量比
(2)该矿石中氧化铁的质量分数为
(3)冶炼生铁的化学方程式为
分析:(1)Fe2O3中铁元素与氧元素的质量比为:(铁的相对原子质量×铁原子个数):(氧的相对原子质量×氧原子个数);
(2)该矿石中氧化铁的质量分数为:赤铁矿石中铁元素的质量分数÷氧化铁中铁元素的质量分数;
(3)生铁冶炼采用的是高温固态还原法,即在炉温提高到1150~1300℃的条件下把铁矿石(氧化铁)还原成铁.据此写出化学方程式.
(2)该矿石中氧化铁的质量分数为:赤铁矿石中铁元素的质量分数÷氧化铁中铁元素的质量分数;
(3)生铁冶炼采用的是高温固态还原法,即在炉温提高到1150~1300℃的条件下把铁矿石(氧化铁)还原成铁.据此写出化学方程式.
解答:解:(1)氧化铁中铁元素与氧元素的质量比为:(56×2):(16×3)=7:3;
(2)该矿石中氧化铁的质量分数为:56%÷
=80%;
(3)生铁冶炼是把铁矿石(氧化铁)还原成铁,还原剂主要是CO,反应的化学方程式为:Fe2O3+3CO
2Fe+3CO2.
故答案为:(1)7:3;(2)80%;(3)Fe2O3+3CO
2Fe+3CO2.
(2)该矿石中氧化铁的质量分数为:56%÷
| 56×2 |
| 160 |
(3)生铁冶炼是把铁矿石(氧化铁)还原成铁,还原剂主要是CO,反应的化学方程式为:Fe2O3+3CO
| ||
故答案为:(1)7:3;(2)80%;(3)Fe2O3+3CO
| ||
点评:本题主要考查学生运用化学式进行计算的能力.同时要知道生铁冶炼采用的是高温固态还原法.

练习册系列答案
相关题目

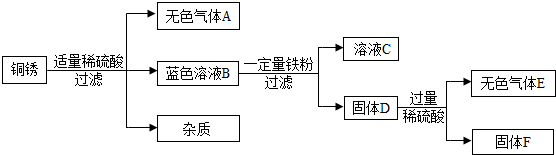

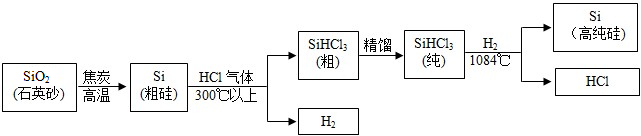
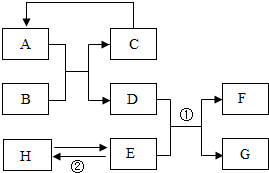 (2013?兰州)已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答:
(2013?兰州)已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答: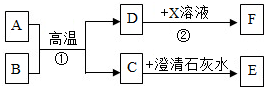 A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B是赤铁矿的主要成分,F是红色固体,其中只有D、F为单质,X为蓝色溶液,它们的转化关系如图所示(部分生成物已省略):
A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B是赤铁矿的主要成分,F是红色固体,其中只有D、F为单质,X为蓝色溶液,它们的转化关系如图所示(部分生成物已省略):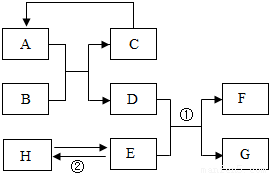 已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答:
已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答: