题目内容
【题目】某化学兴趣小组用下图装置进行Na2CO3的性质实验. 【实验装置】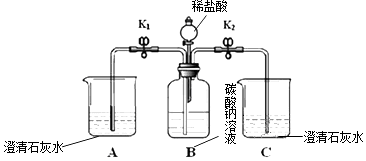
【实验记录】
实验步骤 | 实验现象 | 实验结论 | |
Ⅰ | 向B瓶中滴入几滴酚酞试液 | B瓶中溶液变红 | Na2CO3溶液呈性 |
Ⅱ | 关闭开关K1 , 打开K2 , 并加入一定量稀盐酸 | B中有气泡;C中 | Na2CO3与稀盐酸反应 |
Ⅲ | 关闭开关K2 , 打开K1 | ①B瓶中液体压入A中 | A中发生反应的化学方程式: |
【反思与交流】
①实验后,同学们分析实验Ⅲ中B瓶溶液的溶质为 .
②某同学向B瓶中继续加入稀盐酸,发现A中白色沉淀消失且红色褪去,白色沉淀消失的原因为(用化学方程式表示).
【答案】碱;澄清石灰水变浑浊;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;NaCl和 Na2CO3;CaCO3+2HCl=CaCl2+H2O+CO2↑
【解析】解:【实验记录】碳酸钠显碱性,能使酚酞变红色,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,所以
实验步骤 | 实验现象 | 实验结论 | |
Ⅰ | 向B瓶中滴入几滴酚酞试液 | B瓶中溶液变红 | Na2CO3溶液呈碱性 |
Ⅱ | 关闭开关K1 , 打开K2 , 并加入一定量稀盐酸 | B中有气泡;C中澄清石灰水变浑浊 | Na2CO3与稀盐酸反应 |
Ⅲ | 关闭开关K2 , 打开K1 | ①B瓶中液体压入A中 | A中发生反应的化学方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
【反思与交流】1、实验Ⅲ可知碳酸钠和氢氧化钙反应生成碳酸钙沉淀,所以实验后,同学们分析实验Ⅲ中B瓶溶液的溶质为:NaCl和 Na2CO3;2、碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
【实验记录】Ⅰ碱;Ⅱ澄清石灰水变浑浊;ⅢNa2CO3+Ca(OH)2=CaCO3↓+2NaOH;
【反思与交流】1、NaCl和 Na2CO3; 2、CaCO3+2HCl=CaCl2+H2O+CO2↑.
【考点精析】通过灵活运用书写化学方程式、文字表达式、电离方程式,掌握注意:a、配平 b、条件 c、箭号即可以解答此题.