题目内容
【题目】硅酸钠(Na2SiO3)是我国优先发展的精细化工产品。实验室以5g石英砂粉末(其中SiO2质量分数为96%,其余为不溶于水也不与其他物质反应的杂质)为原料,与一定量NaOH溶液反应制取硅酸钠溶液,反应的方程式为:2NaOH+SiO2Na2SiO3+H2O。充分反应后,过滤,得到硅酸钠溶液20g,将滤渣洗涤、烘干,称量质量为2g。
(1)硅酸钠中钠元素、硅元素的质量比为______________________;
(2)2g滤渣中SiO2的质量质量分数___________;(计算结果精确到0.1%)
(3)求把20g硅酸钠溶液,稀释为质量分数为10%的溶液,求需要加入水的质量_____________;
(4)求原氢氧化钠溶液中溶质的质量分数_____________。(计算结果精确到0.1%)
【答案】23:14 90% 41g 23.5%
【解析】
(1)硅酸钠(![]() )钠元素、硅元素的质量比为(23×2):28=23:14;
)钠元素、硅元素的质量比为(23×2):28=23:14;
(2)5g石英砂粉末(其中![]() 质量分数为96%),则杂质的质量为5g×(1-96%)=0.2g,则2g滤渣中
质量分数为96%),则杂质的质量为5g×(1-96%)=0.2g,则2g滤渣中![]() 的质量为2g-0.2g=1.8g,2g滤渣中
的质量为2g-0.2g=1.8g,2g滤渣中![]() 质量分数为
质量分数为![]() ;
;
(3)由(2)知,反应的二氧化硅的质量为5g-2g=3g,原溶液中氢氧化钠完全反应,原氢氧化钠溶液的质量为20g+2g-5g=17g,设生成的硅酸钠的质量为x,原氢氧化钠溶液中溶质的质量分数为y,则
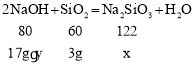
![]()
若把20g硅酸钠溶液,稀释为质量分数为10%的溶液,需要加入水的质量为:![]() ;
;
(4)由(3)知,原氢氧化钠溶液中溶质的质量分数23.5%。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案【题目】为减少温室气体二氧化碳的排放,可以将二氧化碳进行转化。下图为该反应的微观示意图,以下说法成立的是 ( )
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
A.物质C是由离子构成B.以上4种物质中属于氧化物的是A和C
C.反应中C,D两种物质的质量比是1︰2D.该反应属于置换反应
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)保持氢气化学性质的最小粒子是__________。
(2)下图是镁元素和氟元素在元素周期表中的信息。

由此信息得出:
①镁原子的核外电子数是__________;②镁元素与氟元素最本质的区别是__________数不同;③由镁元素与氟元素组成氟化镁的化学式为__________。
(3)A、B、C、D表示四种物质,部分物质的微观示意图见下表。A和B在一定条件下反应生成C和D。
物质 | A | B | C | D |
|
微观示意图 | 纯净物 |
|
|
|
请回答以下问题:
①在B、C、D中属于单质的是__________(填化学式)。
②若一定质量的纯净物A和48g的B恰好完全反应,可生成44gC和27gD,则A的化学式是__________。