题目内容
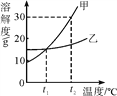
【题目】根据下图提供的几种物质的溶解度曲线,判断下列说法正确的是

A. 氯酸钾中混有少量氯化钠,提纯氯酸钾最好用蒸发结晶的方法
B. 30 ℃时氯酸钾饱和溶液的溶质质量分数为10%
C. 80 ℃时7 g NaCl和20 g水能形成饱和溶液
D. 控制温度,图中氯酸钠和氯化钾能发生化学反应
【答案】A
【解析】由图中信息知,A、氯酸钾溶解度受温度影响较大,氯化钠溶解度受温度影响变化不大,氯酸钾中混有少量氯化钠,提纯氯酸钾最好用蒸发结晶的方法,故A正确;B、30 ℃时氯酸钾溶解度是10g,饱和溶液的溶质质量分数为![]() ×100%=9.1%,故B错误;C、80 ℃时,NaCl溶解度约38g,7 g NaCl和20 g水不能形成饱和溶液,故C错误;D、控制温度,图中氯酸钠和氯化钾不能发生化学反应,故D错误。
×100%=9.1%,故B错误;C、80 ℃时,NaCl溶解度约38g,7 g NaCl和20 g水不能形成饱和溶液,故C错误;D、控制温度,图中氯酸钠和氯化钾不能发生化学反应,故D错误。
点睛∶溶解度曲线的意义⑴表示同一种物质在不同温度时的溶解度或溶解度随温度变化的情况;⑵表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小。若两种物质的溶解度曲线相交,则在该温度下两种物质的溶解度相等;⑶根据溶解度曲线可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法;⑷根据溶解度曲线能进行有关的计算。

练习册系列答案
相关题目