题目内容
在电缆生产过程中会产生一定量的含铜废料。据报道,在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜。反应的化学方程式:2Cu + 2H2SO4 + O2
 2CuSO4
+ 2H2O取一定量溶质的质量分数为10%的稀硫酸(其中含溶质49 g),与铜恰好完全反应,假设其他杂质不反应也不溶解,则反应后硫酸铜溶液中溶质的质量分数是多少?
2CuSO4
+ 2H2O取一定量溶质的质量分数为10%的稀硫酸(其中含溶质49 g),与铜恰好完全反应,假设其他杂质不反应也不溶解,则反应后硫酸铜溶液中溶质的质量分数是多少?
【答案】
15.1%
【解析】
试题分析:设参加反应的铜的质量为x,消耗氧气的质量为y,生成硫酸铜的质量为z
2Cu + 2H2SO4 + O2  2CuSO4
+ 2H2O
2CuSO4
+ 2H2O
128 196 32 320
 49g
49g 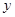

 =32g
=32g 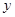 =8g
=8g
 =80g
=80g
溶液质量为
反应后硫酸铜溶液中溶质的质量分数是
考点:化学方程式的计算
点评:化学方程式的计算属于中考必考题型,一般在计算题的最后一道题里面,较为简单,但注意要细心,尤其是计算质量分数。

练习册系列答案
相关题目
 2CuSO4+______
2CuSO4+______