题目内容
【题目】化学小组同学在加热二氧化锰样品时,发现有气泡产生(如图所示),于是他们对这个异常现象进行了探究. 
(1)对气体成分的探究:加热二氧化锰样品,用燃着的木条靠近试管口,木条熄灭.将气体通入澄清的石灰水,发现石灰水变浑浊,产生的气体是 .
(2)对气体来源的探究: 【假设1】甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
实验步骤及现象 | 结论 |
假设不成立. |
【假设2】乙同学认为:二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体.他设计了如图二所示的实验进行研究,其中B装置的作用是检验A中反应是否完全,B中的试剂是 , 实验中观察到D处澄清石灰水变浑浊.他又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现D处澄清的石灰水也变浑浊.
(3)【结论】通过乙同学的实验证明,二氧化锰中混有炭粉,炭粉与反应产生了这种气体.
【答案】
(1)二氧化碳
(2)加热空的试管,另一端的澄清石灰水没有变浑浊;澄清石灰水
(3)二氧化锰
【解析】解:(1)根据二氧化碳能使澄清石灰水变浑浊的特性,可知气体是二氧化碳;(2)加热空的试管,另一端的澄清石灰水没有变浑浊,说明气体不是来自于空气;图二中A是除去空气中的二氧化碳,可以用氢氧化钠溶液,B是验证二氧化碳是否被除净;(3)如果D中石灰水变浑浊,说明乙同学的假设成立,从而得到炭粉与二氧化锰反应生成了二氧化碳. 所以答案是:(1)二氧化碳;(2)【假设2】澄清石灰水;(3)【结论】二氧化锰.
【考点精析】解答此题的关键在于理解碳的化学性质的相关知识,掌握各种单质碳的化学性质却完全相同;1、常温下的稳定性强2、可燃性:完全燃烧(氧气充足),生成CO2;不完全燃烧 (氧气不充足),生成CO;3、还原性:应用:冶金工业;现象:黑色粉末逐渐变成光亮红色,石灰水变浑浊.

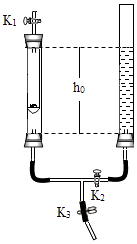
【题目】利用下图装置进行实验(两支玻璃管内径相同).实验前K1、K2、K3均已关闭.
实验装置 | 【实验1】制备气体 | 【实验2】测定空气中氧气含量 |
| 左管中带孔的燃烧匙盛有足量锌粒,右管盛有稀硫酸 | 左管中燃烧匙盛有足量白磷,右管盛有水 |
(1)实验1:锌与稀硫酸反应的化学方程式为;为使反应停止,Ⅲ中的操作是 .
(2)实验2:打开K2 , 右管中液面下降,原因是;计算空气中氧气体积分数的表达式为(用h0、h1表示).