题目内容
【题目】如图是A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
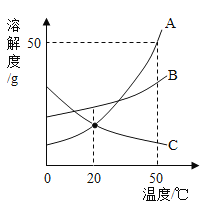
A. 50℃时A B C三种物质的溶解度由大到小的顺序是A>B>C
B. 50℃时把50gA放入100g水中能得到A的不饱和溶液
C. 将C的饱和溶液变为不饱和溶液,可采用降温方法
D. 可以通过冷却热饱和溶液的方法得到A的晶体
【答案】B
【解析】
根据溶解度曲线图可知:物质在不同温度下的溶解度或溶解度随温度变化的情况,判断结晶的方法。
A、50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C,故A正确;
B、50℃时A的溶解度为50g,固体溶解度表示在一定温度下,100g溶剂中溶解的溶质的质量,所以50gA放入100g水中能得到A的饱和溶液,故B不正确;
C、C的溶解度随温度的升高而减少,所以将C的饱和溶液变为不饱和溶液,采取降温的方法,也可以采用加溶质的方法,故C正确;
D、A的溶解度随温度的升高而增大,则可以通过冷却热饱和溶液的方法得到A的晶体,故D正确;故选B。

【题目】复方氢氧化镁片[有效成分Mg(OH)2]和复方碳酸镁片[有效成分MgCO3]是两种常见的抗胃酸药。从A或B中任选一个作答,若均作答,按A计分。
A | B |
(1)Mg(OH)2的相对分子质量为___________。 (2)用复方碳酸镁片治疗胃酸过多症时,反应的化学方程式为_____________。 | (1)MgCO3中氧元素质量分数的计算式为___________。 (2)用复方氢氧化镁片治疗胃酸过多症时,反应的化学方程式为__________。 |
【题目】依据下列实验数据和溶解度曲线完成下面小题。
① | ② | ③ | ④ | |
温度 | 10℃ | 10℃ | 30℃ | 30℃ |
固体种类 | KNO3 | NaCl | KNO3 | NaCl |
固体质量 | 30g | 30g | 40g | 40g |
水的质量 | 100g | 100g | 100g | 100g |
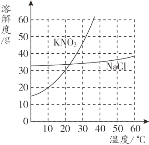
【1】①~④所得的溶液中,属于饱和溶液的是
A. ①和②B. ②和③C. ③和④D. ①和④
【2】下列说法中,正确的是
A. 溶质质量:①=②B. 溶液质量:②>③
C. 溶质质量分数:③>④D. 溶质与溶剂质量比:①=③