ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΡ≥Ά§―ß‘ΎΉωΓΑΝρ‘Ύ―θΤχ÷–»Φ…’Γ±ΒΡ Β―ι ±Θ§ΈΣΝΥΖά÷ΙΩ’ΤχΈέ»ΨΘ§”Ο«β―θΜ·ΡΤ»ή“Κ ά¥Έϋ ’Εΰ―θΜ·ΝρΓΘœ¬Οφ «ΗΟΆ§―ß Β―ι”κΦΤΥψΙΐ≥ΧΘΚ
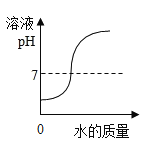
Θ®1Θ©≈δ÷Τ50g»ή÷ ÷ ΝΩΖ÷ ΐΈΣ5%ΒΡ«β―θΜ·ΡΤ»ή“ΚΓΘ”ΟΧλΤΫ≥Τ»Γ_____gΒΡ«β―θΜ·ΡΤΘ§Ζ≈»κ…’±≠÷–Θ§”Ο_____Θ®Χν“«ΤςΟϊ≥ΤΘ©ΝΩ»ΓΘ®Υ°ΒΡΟήΕ»ΈΣ1g/cm3Θ©_____mLΥ°Θ§Φ”»κ…œ ω…’±≠÷–Θ§ΫΝΑηΘ§Άξ»Ϊ»ήΫβΘ§±Η”ΟΓΘ
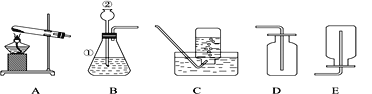
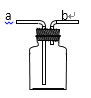
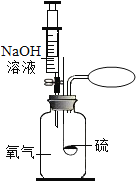
Θ®2Θ©»γΆΦΥυ ΨΘ§Νρ»Φ…’ΚσΘ§”Ο’κΆ≤ΫΪΥυ≈δ÷ΤΒΡNaOH»ή“ΚΉΔ»κΦ·ΤχΤΩ÷–ΓΘ»τΦ·ΤχΤΩ÷–…ζ≥…0.32gΒΡΕΰ―θΜ·ΝρΘ§ΫΪΤδΆξ»ΪΈϋ ’Θ§’κΆ≤“ΣΈϋ»Γ«β―θΜ·ΡΤ»ή“ΚΒΡ÷ ΝΩΈΣ________ΘΩΘ®ΦΌ…η NaOH »ή“ΚΈϋ ’SO2 ±÷ΜΖΔ…ζ»γœ¬Ζ¥”ΠΘΚSO2+2NaOHΘΫNa2SO3+H2OΘ©
ΓΨ¥πΑΗΓΩ2.5 50mLΝΩΆ≤ 47.5 8g
ΓΨΫβΈωΓΩ
Θ®1Θ©≈δ÷Τ50g»ή÷ ÷ ΝΩΖ÷ ΐΈΣ5%ΒΡ«β―θΜ·ΡΤ»ή“ΚΘ°”ΟΧλΤΫ≥Τ»Γ«β―θΜ·ΡΤΒΡ÷ ΝΩ «ΘΚ50gΓΝ5%ΘΫ2.5gΘ§‘ρ–η“Σ Υ°ΒΡ÷ ΝΩ «50g©¹2.5gΘΫ47.5gΘ§Υ°ΒΡΟήΕ»ΈΣ1g/cm3Θ§Κœ47.5mLΘ§”Ο50mLΝΩΆ≤ΝΩ»ΓΘΜ
Θ®2Θ©…ηΈϋ»Γ«β―θΜ·ΡΤΒΡ÷ ΝΩ «x
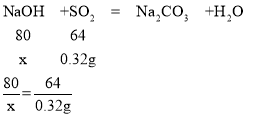
xΘΫ0.4g
‘ρΈϋ»Γ«β―θΜ·ΡΤ»ή“ΚΒΡ÷ ΝΩΈΣ0.4gΓ¬5%ΘΫ8g
Ι ¥πΑΗΈΣΘΚΘ®1Θ©2.5ΘΜ50mLΝΩΆ≤ΘΜ47.5ΘΜ
Θ®2Θ©8gΘ°

ΓΨΧβΡΩΓΩΗυΨί»γΆΦΥυ ΨΒΡ–≈œΔΘ§ΜΊ¥πΘΚ
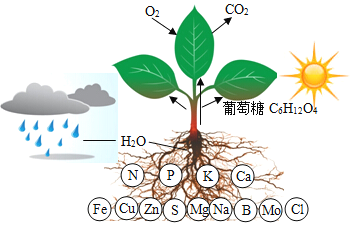
Ή ΝœΘΚΒΊΩ«÷–Κ§ΝΩΫœΕύΒΡ‘ΣΥΊΖ÷≤Φ±μ
‘ΣΥΊ | O | Si | Al | Fe | Ca | ΤδΥϊ |
Ζ÷≤Φ/% | 46.6 | 27.7 | 7.7 | 4.8 | 3.5 | 9.7 |
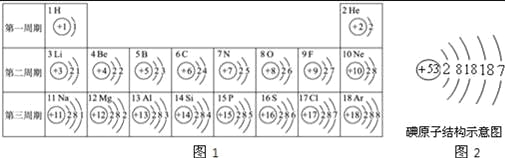
Θ®1Θ©¥”ΆΦ÷–÷ΣΒάNΓΔPΓΔKΚΆCa «÷≤Έο–η“ΣΫœΕύΒΡ”Σ―χ‘ΣΥΊΘ§ΒΪΆ®≥Θ«ιΩωœ¬Θ§Έ“Ο«Ϋœ…ΌœρΆΝ»ά ©”ΟΗΤΖ ΒΡ‘≠“ρ «_____Θ§–¥≥ω“Μ÷÷Κ§ΦΊΒΡΗ¥ΚœΖ ΒΡΜ·―ß Ϋ_____Θ°
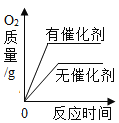
Θ®2Θ©‘Ύ―τΙβ’’…δœ¬Θ§“ΕΤ§…œΚœ≥…ΤœΧ―Χ«ΥυΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «_____Θ§¥ΥΙΐ≥Χ «ΫΪΧΪ―τΡήΉΣΜ·ΈΣ_____ΡήΘ°
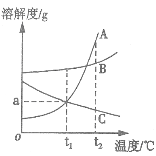
ΓΨΧβΡΩΓΩΡ≥–Υ»Λ–ΓΉι”Ο»γΆΦΥυ ΨΉΑ÷Ο÷Τ»Γ―θΤχΘ§ ‘Ιή÷–ΙΧΧεΒΡ÷ ΝΩΥφ ±Φδ±δΜ·ΒΡ ΐΨίΦϊœ¬±μΓΘ÷Τ»ΓΫα χΚσΘ§ΫΪ Θ”ύΙΧΧε”Ο ΝΩΥ°≥δΖ÷»ήΫβΚσΘ§Ιΐ¬ΥΘ§ΜΊ ’Εΰ―θΜ·ΟΧΙΧΧεΘ§≤ΔΒΟΒΫ¬»Μ·ΦΊ»ή“Κ100gΓΘ
Φ”»» ±Φδ/min | 0 | t1 | t2 | t3 |
ΙΧΧε÷ ΝΩ/g | 28.0 | 23.2 | 18.4 | 18.4 |
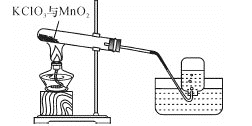
Θ®1Θ©Ι≤÷ΤΒΟ―θΤχ_________gΓΘ
Θ®2Θ©ΦΤΥψΥυΒΟ¬»Μ·ΦΊ»ή“ΚΒΡ»ή÷ ÷ ΝΩΖ÷ ΐ_________ΓΘ