题目内容
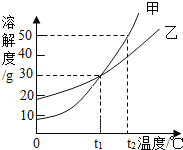
【题目】如图为A、B、C三种固体物质的溶解度曲线。据图回答下列问题。
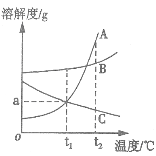
(1)在t1℃时,A、C两物质的溶解度相等,都为____克;
(2)在t2℃时,三种物质中溶解度最大的是________ ;
(3)分别将t2℃时A、B、C三种物质的饱和溶液降温 到t1℃,所得溶液中溶质质量分数由大到小的顺序 是 _______。
【答案】a A B>A>C
【解析】
(1)在t1℃时,A、C两物质的溶解度相等,都为ag,因为在该温度下A、C有交点;
(2)根据溶解度曲线可知,在t2℃时,三种物质中溶解度最大的是A;
(3)将t2℃时A、B、C三种物质的饱和溶液降温到t1℃时,A、B的溶解度减小,C的溶解度随温度的降低而增大,A、B有晶体析出,质量分数变小溶液仍为饱和溶液,C没有晶体析出,质量分数不变,一定温度下饱和溶液的溶质质量分数=![]() ,溶解度越大,质量分数越大,t1℃时B的溶解度大于A的溶解度大于t2℃时C的溶解度,所以t1℃时三种物质的溶质质量分数由大到小的顺序是B>A>C。
,溶解度越大,质量分数越大,t1℃时B的溶解度大于A的溶解度大于t2℃时C的溶解度,所以t1℃时三种物质的溶质质量分数由大到小的顺序是B>A>C。

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组要用80克10%的氢氧化钠溶液来制作“叶脉书签”,如图是他配置氢氧化钠溶液的操作示意图.
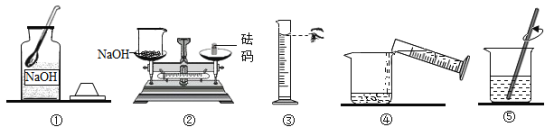
(1)称量氢氧化钠固体时,不能将固体直接放在纸上称量的原因是__;
(2)在配置上述溶液时,下列操作失误,会引起溶质质量分数降低的是__;
a用量筒量取水时,仰视读数
b将量筒中的水倒入烧杯中时,有少量的水溅出
(3)一周后,化学兴趣小组整理实验室时,发现上周实验时取用氢氧化钠固体后忘记盖上瓶盖,老师告知,此瓶氢氧化钠固体已经变质,但未知变质程度,为此,该化学兴趣小组在老师的指导下进行有关实验探究.
(查阅资料)CaCl2溶液和BaCl2溶液都呈中性
(提出问题)
①氢氧化钠固体变质的原因?用化学方程式表示__;
②氢氧化钠固体变质程度如何?
(实验设计)
化学兴趣小组分成甲、乙两组进行实验探究.
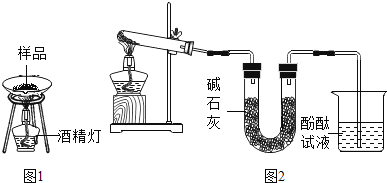
甲组方案:取少量固体样品于烧杯中,加蒸馏水完全溶解,然后滴入Ca(OH)2溶液,直到不再产生沉淀为止,静置,滴入无色酚酞试液,溶液变红,说明氢氧化钠固体部分变质.
乙组不同意甲组的观点,请说明理由:__.
乙组方案:根据如下提供的药品设计实验方案,请你完成下表.
提供的药品:酚酞试液,CaCl2溶液,Ca(OH)2溶液,稀盐酸,BaCl2溶液,蒸馏水.
实验操作步骤 | 实验现象 | 结论 |
a.取少量氢氧化钠固体样品于试管中 b.加蒸馏水完全溶解 c.__ d.__ | __; __ | 氢氧化钠固体部分变质 |