题目内容
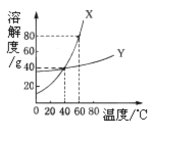
【题目】X、Y两种固体物质的溶解度曲线如图所示,据此小明同学做出了下列分析,其中错误的是
A.在同一温度下,不能配制出溶质质量分数相同的X、Y两种溶物质的饱和溶液
B.60°C时,把40g的X加入50g水中,充分溶解,得到该温度下X的水溶液是饱和溶液
C.当温度大于40°C时,相同温度下X的溶解度大于Y的溶解度
D.40°C时,X、Y两种物质的溶解度都是40g
【答案】A
【解析】
A、根据溶解度曲线可知,40℃时X、Y两种物质的溶解度相等,一定温度下饱和溶液的溶质质量分数=![]() ,所以在40℃时,可以配制出溶质质量分数相同的X、Y两种物质的饱和溶液,故A错误;
,所以在40℃时,可以配制出溶质质量分数相同的X、Y两种物质的饱和溶液,故A错误;
B、60℃时,X物质的溶解度是80g,根据溶解度概念可知,把40g的X加入50g水中,充分溶解,到该温度下X的水溶液是饱和溶液,故B正确;
C、根据溶解度曲线可知,当温度大于40℃时,X的溶解度大于Y的溶解度,故C正确;
D、根据溶解度曲线可知,40℃时,X、Y两种物质的溶解度都是40g,故D正确。故选A。

【题目】请用H、C、O、C1、Na、Fe六种元素中的一种或几种元素,按要求完成下列表格中空格内容:
(1)请写出由,上述六种元素中的一种或几种粒子,构成符合下列要求的粒子的化学符号 | ||
信息要求 | ①两个氢原子 | ③两个铁离子 |
化学符号 | _______ | ________ |
(2)请写出由上述六种元素中的一种或几种元素,组成符合下列要求的物质的化学式 | ||
信息要求 | ①相对分子质量最小的有机物 | ②纯碱 |
化学式 | _______ | ________ |
(3)用上述元素中的一种或几种元素组成物质,写出符合下列要求的一个化学反应方程式 | ||
信息要求 | ①金属氧化物与水化合生成碱溶液 | ②难溶性的碱受热分解 |
方程式 | ________ | ________ |
【题目】Mg(OH)2是一种新型的阻燃剂,在温度达到380°C时吸收热量并分解产生水,同时生成的氧化镁附着于可燃物的表面阻止了进一步燃烧。
(1)Mg(OH)2 受热分解化学方程式是________________;工业常用氯化镁溶液与烧碱溶液制取Mg(OH)2,化学方程式是___________________。
(2)某同学用氨水在实验室模拟制取Mg(OH)2的过程:一定温度下,往含一定量氯化镁的溶液中加入适量氨水( 氨水易挥发),再经过滤、洗涤得到Mg(OH)2晶体。为探究获得较高Mg(OH)2晶体转化率条件,该同学进行如下对比实验,数据如下:
实验编号 | 氯化镁溶液溶质质量分数 | 反应温度/°C | Mg(OH)2转化率/% |
a | 10% | 30 | 27.06 |
b | 15% | 30 | 56.77 |
c | 15% | 40 | 69.64 |
d | 15% | 60 | 54.30 |
e | 20% | 60 | 50.60 |
①实验b和c的目的是______________________。
②由实验可知,能够得到最多Mg(OH)2的条件是溶质质量分数_______和温度__________°C。
③在氯化镁溶液溶质质量分数都是15%的情况下,60°C 时Mg(OH)2的转化率比40°C时低的原因是________________。
(3)根据燃烧的条件可知,Mg(OH)2能做阻燃剂的原因是________________(填编号)。
①清除可燃物 ②使温度 降低到着火点以下 ③隔绝空气
(4)氯化镁溶液通过循环利用,理论上转化率可以达到100%。若生产了2.9吨Mg(OH)2,理论上需要原料20%的氯化镁溶液_______________吨。
【题目】为了证明氢氧化钠和稀盐酸反应有新物质生成,兴趣小组的同学进行了下列实验:
(实验目的)证明氢氧化钠溶液与稀盐酸发生了反应且生成了新物质。
(实验原理)___________ (用化学方程式表示)。
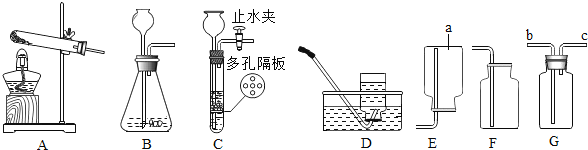
(药品仪器)
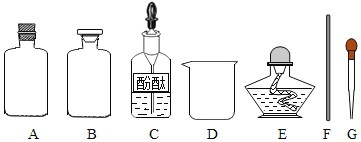
(实验步骤)
①取______(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色。
②用G_______(填仪器名称)向①所得的溶液中滴加稀盐酸,直至红色刚好消失。
③向②所得溶液中继续滴加稍过量稀盐酸,溶液保持无色。
④用F蘸取③所得溶液,在酒精灯上灼烧,有白色固体产生。
(思考拓展)
(1)步骤③的目的是:__________。
(2)进一步确认步骤④所得的白色固体不是氢氧化钠,不能选用的试剂有:_________。
ACuSO4溶液 BNa2CO3溶液 C无色酚酞试液 D(NH4)2SO4溶液
(3)已知酚酞试液在不同pH时的变色情况如下表。
pH | <8.2 | 8.2~10.0 | >10.0 |
颜色 | 无色 | 红色 | 无色 |
小文同学发现向某氢氧化钠溶液中滴加酚酞试液, 发现溶液瞬间变红但立即又变成无色,他接着逐滴加入稀盐酸,某一时刻溶液变红了,没有褪色,继续滴加稀盐酸,后褪至无色。小文认为该氢氧化钠溶液刚开始时滴加酚酞试液出现异常现象的原因,可能是氢氧化钠溶液浓度过大导致的,请你设计实验方案帮助他证明猜想:_________。