题目内容
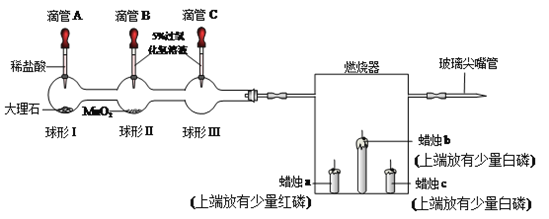
【题目】某校化学兴趣小组的同学利用下图所示装置进行实验.
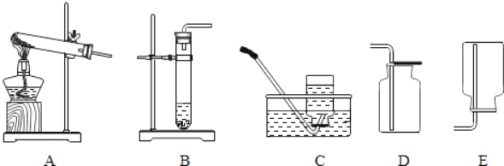
实验目的:
(1)用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验.
(2)粗略测定加热2g高锰酸钾所收集到的氧气体积.
反应原理:(用文字表达式表示)并注明反应类型
高锰酸钾制氧气:_____;_____.
细铁丝在氧气中燃烧:_____;_____.
装置连接:
用高锰酸钾制取并收集一瓶较纯的氧气,应选用_____装置.(填序号)
用分解过氧化氢(H2O2)的方法也能制取氧气,发生装置应选取_____.(填序号)
问题
(1)实验过程发现C瓶中的水变红了,原因是_____.
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能是_____.
【答案】高锰酸钾![]() 锰酸钾+二氧化锰+氧气 分解反应 铁+氧气
锰酸钾+二氧化锰+氧气 分解反应 铁+氧气![]() 四氧化三铁 化合反应 AC B 高锰酸钾粉末被气体吹到水槽中,高锰酸钾溶解在水中从而使水变红 没有在集气瓶的底部加少量水或铺上一层细沙
四氧化三铁 化合反应 AC B 高锰酸钾粉末被气体吹到水槽中,高锰酸钾溶解在水中从而使水变红 没有在集气瓶的底部加少量水或铺上一层细沙
【解析】
反应原理:因高锰酸钾加热分解生成锰酸钾、二氧化锰、氧气,文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气,是一种物质反应生成多种物质,则属于分解反应;因铁和氧气在点燃时生成四氧化三铁,文字表达式为:铁+氧气
锰酸钾+二氧化锰+氧气,是一种物质反应生成多种物质,则属于分解反应;因铁和氧气在点燃时生成四氧化三铁,文字表达式为:铁+氧气![]() 四氧化三铁,是两种物质反应生成一种物质,则属于化合反应;
四氧化三铁,是两种物质反应生成一种物质,则属于化合反应;
装置连接:因高锰酸钾加热分解是固体加热装置,则选A装置,收集较纯净的氧气应采用排水法,则选择C装置;因过氧化氢分解是液体不需要加热的装置,则应选择B装置;
问题(1)因高锰酸钾为紫红色,溶于水而使溶液变红,则可能是高锰酸钾粉末沿导管被气体吹到水槽中;
(2)铁和氧气反应生成的四氧化三铁,温度很高,若直接和集气瓶底部直接接触,会导致集气瓶底部骤热而炸裂,则应事先在集气瓶中加入少量水或铺上一层细沙。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案【题目】在研究金属化学性质的实验中,下列操作不能达到实验目的是![]()
![]()
选项 | 实验目的 | 实验操作 |
A | 证明不同金属与酸反应的剧烈程度不同 | 将铜和银分别放入稀盐酸中 |
B | 研究金属是否都能与盐酸反应 | 将镁、锌、铜片分别放入稀盐酸中 |
C | 证明铜的活动性比银强 | 将铜放入硝酸银溶液中 |
D | 比较锌和铜的金属活动性 | 将锌和铜分别放入稀硫酸中 |
A. AB. BC. CD. D
【题目】对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究CO2通入NaOH溶液是否发生了反应,设计了下列二组实验。请和化学兴趣小组的同学一起探究并回答问题:
(设计与实验)
实验 序号 | 实验步骤一 | 实验步骤二 | 实验 序号 | 实验步骤一 | 实验步骤二 |
实验I |
|
| 实验II |
|
|
(探究与结论)
(1)实验I中步骤一看不到明显现象,步骤二产生的现象是____________________。(2)实验Ⅱ中步骤二看到有白色沉淀析出,则发生反应的化学方程式是__________。
(3)在实验Ⅱ的步骤一中CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是____________________。
(拓展延伸)现有下列信息:
资料卡片一
20℃NaOH、Na2CO3在水中的溶解度
物质 溶解度(S)/g
NaOH 109
Na2CO3 21.8
资料卡片二
20℃NaOH、Na2CO3在乙醇中的溶解度
物质 溶解度(S)/g
NaOH 17.3
Na2CO3 <0.01
请你和化学兴趣小组的同学一起利用以上料信息再设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
实验Ⅲ的操作为:_____________________________。
看到的现象是_________________________________。