题目内容
【题目】下图中A~H和甲、乙、丙分别是初中化学常见的物质。已知甲和G均为黑色固体单质,D是大理石的主要成分,丙常用来配制农药波尔多液,常温下C、E、F均为无色气体(图中有部分生成物未标出)。

请填写下列空白:
(1)写出下列物质的化学式;A_____;F_____;乙_____。
(2)写出下列反应的化学方程式:B→E的反应:_____;G→H的反应:_____。
【答案】Ca(HCO3)2 CO Fe2O3 
![]()
【解析】
A~H和甲、乙、丙分别是初中化学常见的物质,D是大理石的主要成分,可推出D为碳酸钙,A在加热的条件下分解为碳酸钙、B、C,碳酸氢钙能在加热的条件下分解为碳酸钙、二氧化碳和水,可推出A为碳酸氢钙,B在通电的条件下生成E,E能与乙在高温的条件下反应生成G,G为黑色固体单质,常温下C、E、F均为无色气体,可推出B为水,E为氢气,乙可能为三氧化二铁,G为铁,甲为黑色固体单质,C能与甲在高温的条件下反应生成F,F能与乙在高温的条件下反应生成G,可推出C为二氧化碳,甲为碳,F为一氧化碳,丙常用来配制农药波尔多液,且丙能与G反应,可推出丙为硫酸铜。
(1)A为碳酸氢钙,化学式为:Ca(HCO3)2;F为一氧化碳,化学式为:CO;乙可能为三氧化二铁,化学式为:Fe2O3;
(2)B为水,E为氢气,水在通电的条件下分解为氢气和氧气,该反应的化学方程式为: ;
;
G为铁,G→H的反应为铁与硫酸铜反应生成硫酸亚铁和铜,该反应的化学方程式为:![]() 。
。

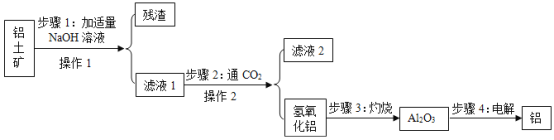
【题目】金属钛广泛用于航空航天工业、化工、医疗等领域。用钛铁矿(主要成分为FeTiO3,同时含有少量的Fe2O3、FeO等)制取钛并获得副产品Fe2O3的主要工艺流程如图所示:
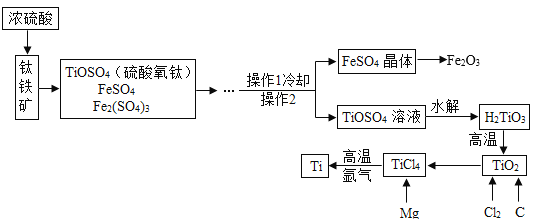
(查阅资料)钛、镁在高温下易与空气中的氧气、二氧化碳等反应。请回答下列问题:
(1)构成金属钛的微粒是_____(填“分子”“原子”或“离子”),H2TiO3中钛元素的化合价为_____;
(2)写出工艺流程中生成硫酸铁的化学方程式_____。
(3)工艺流程中,“水解”属于_____变化(填“化学”或“物理”)。
(4)工业上常在高温和氩气氛围中,用金属镁和TiCl4反应的方法制备Ti,氩气的作用是_____;若反应前钛铁矿中FeTiO3的质量为1.52t,则理论上可以制取Ti的质量为_____t。
(5)已知将FeSO4隔绝空气加强热,可获得Fe2O3,同时产生SO2和SO3.为了降低SO2的产率,提高SO3的产率,某实验小组进行了系列探究,实验数据如下:
编号 | 空气通入量/Ls1 | 温度/℃ | SO2产率/% | SO3产率/% |
a | 0.02 | 850 | 45.4 | 54.6 |
b | 0.06 | 850 | 30.5 | 69.5 |
c | 0.10 | 810 | 11.1 | 88.9 |
d | 0.10 | 850 | 11.1 | 88.9 |
e | 0.10 | 890 | 11.2 | 88.8 |
①本实验主要研究了哪些因素对SO3产率的影响_____。
②根据上表数据,生产过程中采用实验_____(填编号)的提取条件最合理。