题目内容
【题目】下列对分子、原子、离子的认识,正确的是
A.原子是最小的粒子,不可再分
B.相同原子可能构成不同的分子
C.离子不能直接构成物质
D.固体难压缩,说明固体分子间无间隔
【答案】B
【解析】
试题分析:A.原子是最小的粒子,不可再分,是错误的叙述,原子是化学变化中的最小粒子;B.相同原子可能构成不同的分子,是正确的叙述,如氧原子构成氧气、二氧化碳等;C.离子不能直接构成物质 ,是错误的叙述,氯化钠就是由离子构成的; D.固体难压缩,说明固体分子间无间隔,是错误的叙述,说明分子之间的间隔小;故答案选择B

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案【题目】(17分)钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
(2)某钢铁厂每天消耗5000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?
II.实验探究炼铁原理某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4 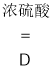 CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;于是他设计了下图的实验装置,结合装置回答下列问题:
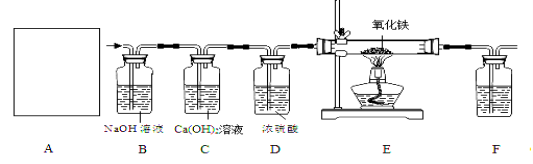
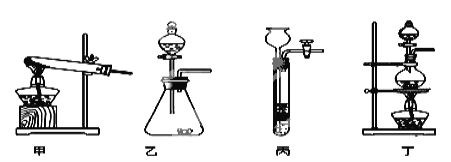
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的澄清石灰水,该反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解。
b.Fe2O3与CO反应的固体生成物可能情况如下:
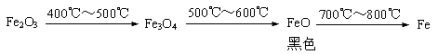
根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
玻璃管质 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 | |
反应前 | 28.20 g | 33.00 g | 300.0 g |
反应后 | 32.84 g | 300.4 g |
根据上述数据,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程)