题目内容
如图1是某试剂瓶标签上的内容.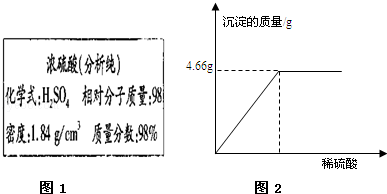
(1)要把10g这种浓硫酸稀释为20%的硫酸,需要水的质量为 39 g.在用量筒量取水时若是仰视读数,将导致稀释后的硫酸溶液质量分数 (“>”、“<”或“=”)20%
(2)试计算用上述稀释用的稀硫酸测定50gBaCl2溶液的质量分数,实验数据如图2所示,写出具体的计算过程.(已知:BaCl2+H2SO4=BaSO4↓+2HCl )
(1)39;<;(2)8.32%.
解析试题分析:(1)设需要加水的质量是x
10g×98%=(10g+x)×20%
x=39g
由于在用量筒量取水时若是仰视读数会导致水量比实际值大,这将导致稀释后的硫酸溶液质量分数小于20%;故填:39;<;
(2)设该50gBaCl2溶液中BaCl2的质量为x,
BaCl2+H2SO4=BaSO4↓+2HCl
208 233
x 4.66g x=4.16g
x=4.16g
该50g BaCl2溶液中BaCl2的质量分数为: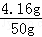 ×100%=8.32%
×100%=8.32%
答:该50g BaCl2溶液中BaCl2的质量分数为8.32%.
考点:根据化学反应方程式的计算;用水稀释改变浓度的方法;有关溶质质量分数的简单计算.

练习册系列答案
相关题目
化学兴趣小组为了测定石灰石中碳酸钙的质量分数(杂质不溶于水,也不与盐酸反应).测得的数据如下:
| 实验组次 | 1 | 2 | 3 | 4 |
| 样品质量/g | 30 | 20 | 20 | 30 |
| 稀盐酸的质量/g | 50 | 50 | 100 | 100 |
| 产生气体的质量/g | 6.6 | 6.6 | 6.6 | m |
(1)m的值为多少?
(2)第 组实验恰好完全反应?
(3)该石灰石样品的纯度是多少?
实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式: _____________________
小倩发现,氯酸钾与氧化铁混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铁外,氧化铜也可以作氯酸钾分解的催化剂.
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
| ③ | 氯酸钾、氧化铁(质量比l:1) | 390 |
| ④ | 氯酸钾、氧化铜(质量比1:1) | 370 |
【分析数据、得出结论】
(1)由实验 与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是________.
【反思】
(1)若要证明氧化铜是该反应的催化剂,还要验证它在化学反应前后质量和____不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证___________________________________________________;



