题目内容
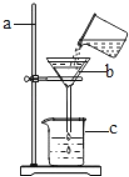
【题目】吴仲良中学初中化学组经常进行有趣的化学实验,其中吹气生火实验吸引了不少同学的关注。用棉花包裹住淡黄色固体过氧化钠(Na2O2),使用玻璃管向棉花内吹气,棉花会燃烧起来,黄色的过氧化钠反应后会变成白色固体.某老师带领化学兴趣小组对白色固体的成分进行了探究.
(查阅资料)
(1)Na2CO3溶液呈碱性;CaCl2溶液呈中性
(2)Na2O2能与水起反应生成氢氧化钠和氧气,也能与二氧化碳起反应生成碳酸钠和氧气.并放出热量
(假设与猜想)根据呼出的气体中含有较多的成分与过氧化钠反应后生成的物质,作出如下猜想:猜想一:氢氧化钠;猜想二:碳酸钠;猜想三:______
(实验验证)
实验步骤 | 实验现象 | 结 论 |
1.小乐同学取少量白色固体于试管中,加水溶解,然后滴加酚酞溶液. | 溶液变红色 | 白色固体中一定含有氢氧化钠. |
2小星同学取少量白色固体于试管中,加入稀盐酸. | 白色固体中一定含有碳酸钠 | |
3小雨同学取少量白色固体于试管中,加水溶解,再加入足量的氯化钙溶液.取上层清夜加入酚酞 | 出现白色沉淀,溶液变红 | 一定含有氢氧化钠 |
步骤2中实验现象为___________________。
(讨论与反思) 聪明的苏苏同学认为小乐同学的实验不能得出这一结论,理由是______。
实验步骤中第3步中产生白色沉淀的反应原理,用化学方程式表示为______。
(得出结论)猜想三成立.
(拓展应用)根据空气的成分和过氧化钠的化学性质,提出保存过氧化钠方法______。
【答案】氢氧化钠和碳酸钠 产生大量气泡 碳酸钠溶液也呈碱性,也能使酚酞溶液变红 ![]() 密封保存
密封保存
【解析】
假设与猜想:
由于呼出的气体中含有二氧化碳和水蒸气,Na2O2能与水起反应生成氢氧化钠和氧气,也能与二氧化碳起反应生成碳酸钠和氧气,故白色固体可能为氢氧化钠、碳酸钠或氢氧化钠与碳酸钠的混合物,故猜想三为:氢氧化钠和碳酸钠;
实验验证:
2、结论为白色固体中一定含有碳酸钠,实验步骤为:小星同学取少量白色固体于试管中,加入稀盐酸,由于碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,有气泡产生,故实验现象为:有气泡产生;
讨论与反思:
碳酸钠也呈碱性,能使无色酚酞试液变红,故不能证明固体中一定含有氢氧化钠;
实验步骤中第3步中产生白色沉淀为氯化钙和碳酸钠反应生成了碳酸钙和氯化钠,该反应的化学方程式为:![]() ;
;
拓展应用:
空气中含二氧化碳和水蒸气,而Na2O2能与水起反应生成氢氧化钠和氧气,也能与二氧化碳起反应生成碳酸钠和氧气,故保存过氧化钠应密封保存。

 全能练考卷系列答案
全能练考卷系列答案【题目】小明在某食品包装袋内发现有一个装有白色颗粒状固体的小纸袋,上面写着(干燥剂,主要成分为生石灰)小明将小纸袋放在空气中,一段时间后,发现纸袋内的白色颗粒黏在一起成为块状。他把块状固体拿到实验室和同学们一起进行实验探究。
(1)请你帮助他们完成实验探究的方案:
实验操作 | 预测实验现象 | 实验结论 | 原因解释 |
①取少量块状固体于试管中,加热至高温,并将生成气体通入澄清石灰水中 | ___ | 有碳酸钙 | 试管中发生的反应方程式为____ |
②另取少量块状固体于试管中,加适量水振荡,静置后,向上层清液中滴加酚酞试液。 | ___ | 块状固体中含有氢氧化钙 |
(2)对这个实验方案①,有同学提出了问题,为什么块状固体中会有碳酸钙呢?请你用方程式做出解释___。
(3)对实验方案②,小明提出了质疑,认为这个实验结论不准确,理由是_____。