题目内容
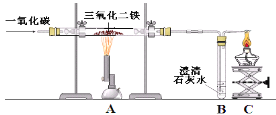
【题目】利用下表中的装置进行实验。有关该实验说法不正确的是( )
实验装置 | 实验步骤 |
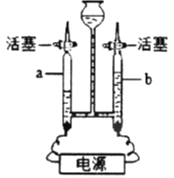
| ①将a试管充满二氧化碳,b试管加入紫色石蕊溶液(K处于关闭状态) ②密闭下,用针筒将a试管中部分二氧化碳抽出 |
A. 用针筒将部分二氧化碳抽出,a试管中气体分子间间隔变大
B. 打开K,b试管中的液体颜色变红
C. 打开K,导管E内液面上升
D. 打开K,发生反应:H2O+CO2==H2CO3
【答案】B
【解析】
A、将部分二氧化碳抽出,二氧化碳减少,试管中气体分子间间隔变大,A项正确;
B、a装置中压强减小,打开K后,E管液面上升,在E处的石蕊能够变红,b试管中的溶液不能变红,B项错误;
C、a试管中的二氧化碳变少,压强减小,打开K后,E管液面会上升,C项正确;
D、二氧化碳和水反应生成碳酸:H2O+CO2==H2CO3,D项正确。
故选择B项。

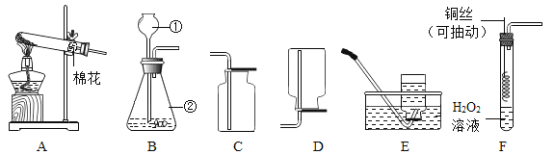
【题目】如图将纸花放入集气瓶中,表格中下列说法不正确的是 ( )
纸花 | 集气瓶中盛放的物质 | 集气瓶中纸花颜色的变化 | |
A | 紫色石蕊浸泡后,晾干的纸花 | 二氧化碳 | 纸花仍为紫色 |
B | 紫色石蕊浸泡后的湿纸花 | 二氧化碳 | 纸花由紫色变为红色 |
C | 紫色石蕊浸泡后的湿纸花 | 少量醋酸 | 纸花由紫色变为红色 |
D | 酚酞溶液浸泡后的湿纸花 | 少量浓氨水 | 纸花由红色变为无色 |
A. A B. B C. C D. D
【题目】小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题。他设计并完成了下表所示的探究实验:
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验一 | 将氯酸钾加热至融化,伸入带火星的木条。 | 木条复燃 | 氯酸钾受热能分解产生氧气,但是速度较慢。 | 二氧化锰是氯酸钾受热分解的催化剂。 |
实验二 | 加热二氧化锰,伸入带火星的木条。 | 木条不复燃 | 二氧化锰受热不产生氧气。 | |
实验三 | 加热氯酸钾与二氧化锰的混合物 | 木条迅速复燃 | 二氧化锰能加快氯酸钾的分解。 | |
(1)在小明不同的探究实验中,实验一和实验二起的作用是__________;
(2)你认为由上述实验能完全得出表内“总结”吗?________(填“能或不能”),其理由是:一、___________;二、____________。
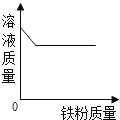
(3)某学生将一定质量的氯酸钾分成a、b两等分,他在a中加入少量二氧化锰混合均匀后将其装入试管中,另一份b直接装入试管中,然后按照要求架设好装置进行氧气的制取.其制取氧气的情况如图所示:
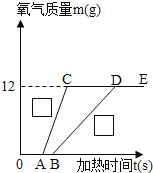
曲线缓则反应慢、曲线陡则反应快,试将a、b标在图中的“□”中_________、______;
点A、点B表示_________,点C、点D表示_________(填“反应开始”或“反应结束”).
OA、OB表示反应前所需的加热时间,依据OB>OA可看出催化剂二氧化锰的存在不仅可以加快化学反应速率,而且还可以______.
图中a、b两种情况的最终氧气产量均为12g,说明催化剂只能改变化学反应速率,不能改变____.
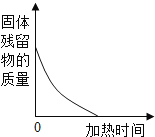
【题目】化学兴趣小组为测定一批石灰石样品中碳酸钙的质量分数,取用20g石灰石样品,进行高温煅烧(样品中除碳酸钙外,其余成分高温不分解。碳酸钙分解的化学方程式为CaCO3 == CaO + CO2↑),不同时间测得剩余固体的质量如下表所示:
煅烧的时间(min) | 剩余固体的质量(g) |
2 | 17.8 |
4 | 13.4 |
6 | 12.3 |
8 | 12.3 |
(1)完全反应后生成二氧化碳的质量_____________。
(2)求石灰石样品中碳酸钙的质量分数_______