题目内容
由于实验室检验二氧化碳用澄清石灰水,不用氢氧化钠溶液,因此小亮同学认为氢氧化钠溶液与二氧化碳不反应,小丽同学不同意小亮同学的观点,认为能反应.请你与他们一起探究,验证小丽同学的观点.
(1)【提出假设】NaOH溶液能与CO2反应.
(2)【实验验证】
(3)【总结反思】实验证明NaOH溶液能与CO2反应.暴露在空气中的NaOH容易变质,其化学方程式为
所以NaOH应 保存.
(4 )现有一些氢氧化钠固体放在敞口烧杯中,为了解这一氢氧化钠固体的变质情况,小丽大胆做出以下猜想:样品可能 ①没有变质 ②完全变质 ③部分变质
小丽和小亮分别用两种实验原理不同的实验证明了此氢氧化钠样品已变质;请你填全表格:
(1)【提出假设】NaOH溶液能与CO2反应.
(2)【实验验证】
| 实验步骤 | 实验现象 | 结论 |
| 向集满CO2的塑料瓶中倒人适量NaOH溶液,立即拧紧瓶盖,振荡 | NaOH溶液吸收了塑料瓶中的CO2气体 | |
| 取上一步骤中所得溶液,加人盐酸 | 化学方程式为: |
(4 )现有一些氢氧化钠固体放在敞口烧杯中,为了解这一氢氧化钠固体的变质情况,小丽大胆做出以下猜想:样品可能 ①没有变质 ②完全变质 ③部分变质
小丽和小亮分别用两种实验原理不同的实验证明了此氢氧化钠样品已变质;请你填全表格:
| 实验人 | 实验步骤 | 实验现象 | 结论 |
| 小丽 | 有气泡产生 | 氢氧化钠已变质 方程式 | |
| 小亮 | 有白色沉淀生成 | 氢氧化钠已变质 方程式 |
考点:探究酸碱的主要性质,药品是否变质的探究,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(2)根据氢氧化钠与二氧化碳反应的结论可知实验现象,再利用碳酸钠与盐酸的反应来分析现象和结论;
(3)根据氢氧化钠溶液不能暴露在空气中,因其极易与空气中的二氧化碳反应而变质,则应密封保存解答;
(4)
小丽:根据酸会与碳酸盐反应生成二氧化碳气体进行设计实验;
小亮:根据加入氢氧化钡溶液,氢氧化钡和碳酸钠反应生成氢氧化钠和碳酸钡沉淀解答;
(3)根据氢氧化钠溶液不能暴露在空气中,因其极易与空气中的二氧化碳反应而变质,则应密封保存解答;
(4)
小丽:根据酸会与碳酸盐反应生成二氧化碳气体进行设计实验;
小亮:根据加入氢氧化钡溶液,氢氧化钡和碳酸钠反应生成氢氧化钠和碳酸钡沉淀解答;
解答:解:
(2)由NaOH溶液吸收了塑料瓶中的CO2气体可知,实验中会观察到塑料瓶变瘪,又氢氧化钠与二氧化碳反应后生成碳酸钠,加入盐酸时会反应生成二氧化碳,则会观察到有气泡冒出,该反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑,故答案为:
(3)由上述实验可知NaOH溶液能与CO2反应,其反应为2NaOH+CO2=Na2CO3+H2O,则氢氧化钠溶液应密封保存,否则容易变质,故答案为:2NaOH+CO2=Na2CO3+H2O;密封.
(4)
小丽:取少量样品加入试管中,滴加稀盐酸,有气泡产生,氢氧化钠已变质,反应的方程式为:Na2C03+2HCl=2NaCl+H2O+CO2↑;
小亮:取少量样品加入试管中,加水溶解,再滴加几滴Ba(OH)2,有白色沉淀生成,氢氧化钠已变质,反应的方程式为:Na2C03+Ba(OH)2=BaC03↓+2NaOH.
答案:
(2)
(3)2NaOH+C02=Na2C03+H2O 密封保存
(4)
(2)由NaOH溶液吸收了塑料瓶中的CO2气体可知,实验中会观察到塑料瓶变瘪,又氢氧化钠与二氧化碳反应后生成碳酸钠,加入盐酸时会反应生成二氧化碳,则会观察到有气泡冒出,该反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑,故答案为:
| 实验步骤 | 实验现象 | 结 论 |
| 塑料瓶变瘪 | ||
| 有气泡产生 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
(4)
小丽:取少量样品加入试管中,滴加稀盐酸,有气泡产生,氢氧化钠已变质,反应的方程式为:Na2C03+2HCl=2NaCl+H2O+CO2↑;
小亮:取少量样品加入试管中,加水溶解,再滴加几滴Ba(OH)2,有白色沉淀生成,氢氧化钠已变质,反应的方程式为:Na2C03+Ba(OH)2=BaC03↓+2NaOH.
答案:
(2)
| 验步骤 | 实验现象 | 结论 |
| 向集满CO2的塑料瓶中倒人适量NaOH溶液,立即拧紧瓶盖,振荡 | 塑料瓶变瘪 | NaOH溶液吸收了塑料瓶中的CO2气体 |
| 取上一步骤中所得溶液,加人盐酸 | 有气泡放出 | 化学方程式为:Na2C03+2HCl=2NaCl+H2O+CO2↑ |
(4)
| 实验人 | 实验步骤 | 实验现象 | 结论 |
| 小丽 | 取少量样品加入试管中,滴加稀盐酸 | 有气泡产生 | 氢氧化钠已变质 方程式 Na2C03+2HCl=2NaCl+H2O+CO2↑ |
| 小亮 | 取少量样品加入试管中,加水溶解,再滴加几滴Ba(OH)2 | 有白色沉淀生成 | 氢氧化钠已变质 方程式 Na2C03+Ba(OH)2=BaC03↓+2NaOH |
点评:本题考查了氢氧化钠溶液与二氧化碳的反应,利用气体体积的变化说明发生了化学反应,并利用性质来说明该物质的保存,学生应注意物质的性质、实验现象、实验结论之间的关系来解答.

练习册系列答案
相关题目
下列有关溶液的说法中正确的是( )
| A、溶液都是无色透明的混合物 |
| B、饱和溶液不一定是浓溶液,不饱和溶液一定是稀溶液 |
| C、36gNaCl溶液在100g水中刚好形成饱和溶液,故NaCl的溶解度为36g |
| D、将1g某物质加入到9g水中,所得溶液的溶质质量分数不一定是10% |
下列有关分子、原子和离子的说法正确的是( )
| A、保持氯气化学性质的粒子是氯原子 |
| B、分子、原子和离子都不显电性 |
| C、氯化钠是由离子组成的 |
| D、分子间有一定间隔,原子间没有间隔 |
如图中“ ”和“
”和“ ”分别表示不同的原子,其中表示化合物的是( )
”分别表示不同的原子,其中表示化合物的是( )
 ”和“
”和“ ”分别表示不同的原子,其中表示化合物的是( )
”分别表示不同的原子,其中表示化合物的是( )A、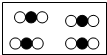 |
B、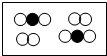 |
C、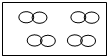 |
D、 |
如图为某化学反应的微观示意图,其中“●”和“○”表示不同元素的原子,下列说法错误的是( )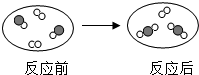

| A、化学反应前后原子个数不变 |
| B、生成物是氧化物 |
| C、生成物的每个分子由三个原子构成 |
D、参加反应的 和 和 的个数比为2:1 的个数比为2:1 |
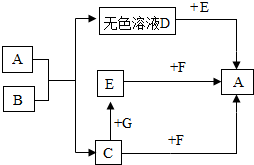 图中的A、B、C、D、E、F、G都是初中化学中的常见物质.其中A是一种盐,常用作建筑材料,B是人体胃液中所含的一种酸,C是植物光合作用的一种原料,E是盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产等,F、G是碱.它们之间存在以下转化关系(图中部分生成物已略去).
图中的A、B、C、D、E、F、G都是初中化学中的常见物质.其中A是一种盐,常用作建筑材料,B是人体胃液中所含的一种酸,C是植物光合作用的一种原料,E是盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产等,F、G是碱.它们之间存在以下转化关系(图中部分生成物已略去).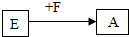 的化学反应方程式:
的化学反应方程式: