题目内容
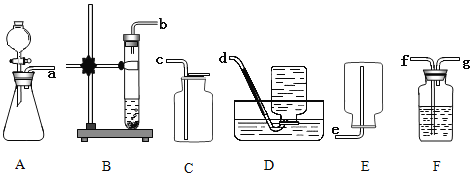
【题目】下列各图表示初中化学常见的四个实验,回答下列问题:
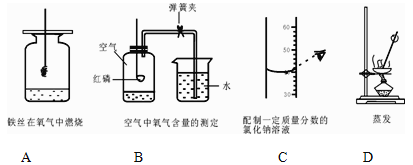
(1)A实验中集气瓶内预先装少量水的目的是 。
(2)B实验中导致实验结果偏大的原因是 (只写一个)。
(3)C实验中该操作将导致所配溶液溶质质量分数 (填“偏大”“偏小”或“不变”)。
(4)D实验中玻璃棒的作用是 。
【答案】(1)防止熔化物溅落下来炸裂瓶底。
(2)弹簧夹没夹紧(或点燃的红磷伸入集气瓶后,没有迅速塞紧橡皮塞)。
(3)偏大
(4)搅拌,防止因局部温度过高,造成液滴飞溅。
【解析】
试题分析:(1)铁丝在氧气中燃烧放出大量的热
(2)弹簧夹没夹紧(或点燃的红磷伸入集气瓶后,没有迅速塞紧橡皮塞),使一部分空气逸出
(3)俯视读数使量取的水偏少,导致所配溶液溶质质量分数偏大
(4)搅拌,防止因局部温度过高,造成液滴飞溅。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
【题目】将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:
物质 | a | b | c | d |
反应前的质量/g | 6.4 | 14.0 | 3.2 | 1.0 |
反应一段时间后的质量/g | 10.0 | 7.2 | x | 1.0 |
下列有关说法正确的是
A. a和b是反应物 B. x=3.2
C. d一定是催化剂 D. 该反应属于分解反应
【题目】一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 | A | B | C | D |
反应前质量/g | 1.7 | 2.2 | 7.9 | 0.9 |
反应后质量/g | 待测 | 6.6 | 0 | 2.7 |
则反应后A的质量为___________;该反应中B和D两种物质变化的质量比为_______。