题目内容
【题目】三聚氰胺(C3H6N6)是一种重要的化工原料,可由尿素[CO(NH2)2]发生如下反应制取:
6 CO(NH2)2 ![]() C3H6N6+6X↑+3CO2↑。推断并计算:
C3H6N6+6X↑+3CO2↑。推断并计算:
⑴根据化学方程式推断:X的化学式为________________;
⑵制取12.6g三聚氰胺,最少需要尿素的质量;
⑶三聚氰胺中氮元素的质量分数。(结果精确到0.1%)
⑷蛋白质中氮元素的质量分数平均为16%,16g三聚氰胺与多少克蛋白质的含氮量相当?
【答案】(1)NH3 ⑵36g (3)66.7% (4)66.7g
【解析】
试题分析:(1)根据质量守恒定律的微观解释:化学反应前后,原子的种类、个数都不变,结合反应:
6 CO(NH2)2 ![]() C3H6N6+6X↑+3CO2↑,不难推出X的化学式为NH3
C3H6N6+6X↑+3CO2↑,不难推出X的化学式为NH3
(2)根据化学方程式中C3H6N6与CO(NH2)2的质量关系,即可求解
设尿素的质量为x
6CO(NH2)2 ![]() C3H6N6 +6X↑+3CO2↑
C3H6N6 +6X↑+3CO2↑
360 126
x 12.6 g
360/x=126/12.6 g x=36 g
(3)根据化学式C3H6N6,三聚氰胺中氮元素的质量分数=14×6/(12×3+1×6+14×6) ×100% = 66.7%
(4)根据元素质量=物质质量×元素的质量分数的表达式
解: 设蛋白质的质量为y
16 g×66.7%=y×16% y= 66.7 g
答:最少需要尿素的质量是36 g;三聚氰胺中氮元素的质量分数是66.7%;16 g三聚氰胺与66.7 g蛋白质的含氮量相当

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】(12分)小李在化学实验技能考查中,完成“用稀盐酸鉴别氢氧化钠溶液和碳酸钠溶液,并测碳酸钠溶液的pH”实验。
【实验一】小李取待测液甲、乙分别放置在试管①和②,再往两支试管中滴入稀盐酸,观察实验现象。根据现象推知,乙为碳酸钠溶液。
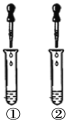
(1)实验中,小李应观察到试管②的现象是__________________________________,
该试管中反应的化学方程式为_________________________________。
(2)老师指出:除盐酸外,还可使用其它试剂鉴别氢氧化钠和碳酸钠溶液。请你选择一种不属于酸的试剂,并将鉴别实验中的预期现象以及化学方程式填入下表。
选择的试剂 | 预期现象 | 反应的化学方程式 |
____________ | 一支试管无明显现象; 另一支试管________________ | _________________________ |
【实验二】小李用玻璃棒蘸取“实验一”后试管②中的溶液沾在pH试纸上,观察试纸颜色变化并与标准比色卡对照,读出溶液的pH。小李的记录如下:
实验现象 | 结论 |
溶液沾在试纸上时,试纸缓慢地变色 | 与标准比色卡对比,Na2CO3溶液pH=3 |
(3)小李因操作错误,得出“Na2CO3溶液pH=3”的错误结论。指出小李操作错误之处。
答:_______________________________________________________________。
(4)指出小李记录的“实验现象”中不科学的地方。
答:_______________________________________________。