题目内容
【题目】向Mg(HCO3)2溶液中加入一定量NaOH溶液,出现白色沉淀.某同学经过过滤、洗涤、低温烘干得白色固体,并作如下探究: 【猜测】
白色固体可能是:①Mg(OH)2;②MgCO3;③Mg(OH)2、MgCO3混合物.
【资料】
MgCO3、Mg(OH)2加热易分解,生成对应的两种氧化物.
【实验1】
(1)取适量白色固体,溶于 , 出现(填现象),则猜测①不成立.
(2)另取适量白色固体,充分加热,产生的气体使无水CuSO4粉末变蓝,则猜测(选填“②”或“③”)成立. 有同学查阅资料得知上述固体应为碱式碳酸镁[xMgCO3yMg(OH)23H2O],其不溶于水,加热易分解.
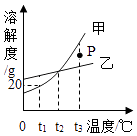
(3)【实验2】 为进一步确定白色固体的组成,该同学取适量白色固体,充分加热至质量不再改变,并使产生的气体全部缓缓通过如图(选填“甲”或“乙”)装置,测得生成气体的质量.
实验数据:
①加热后剩余固体质量1.60g;
②浓硫酸增重0.72g;
③浓NaOH溶液增重1.32g.
则:x:y= .
(4)【延伸】 将该碱式碳酸镁长期浸泡在浓NaOH溶液中,固体全部转化为Mg(OH)2 . 写出此反应的化学方程式 .
(5)工业上碱式碳酸镁可作阻燃剂,其可能的原因是(选填序号). a、分解时吸热,降低可燃物的着火点
b、生成的固体覆盖燃烧物,隔绝氧气
c、生成的气体稀释了可燃物周围的氧气浓度.
【答案】
(1)稀盐酸(或稀硫酸或稀硝酸等);气泡
(2)③
(3)甲;3:1
(4)3MgCO3?Mg(OH)2?3H2O+6NaOH=4Mg(OH)2↓+3Na2CO3+3H2O
(5)bc
【解析】解:(1)猜想①不成立,也就是白色固体中含有碳酸镁,作为一种碳酸盐能与酸反应生成二氧化碳气体;故填:稀盐酸(或稀硫酸或稀硝酸等);气泡;(2)因为MgCO3、Mg(OH)2加热易分解,生成对应的两种氧化物,也就是碳酸镁加热分解为氧化镁和二氧化碳;氢氧化镁加热分解为氧化镁和水;充分加热,产生的气体使无水CuSO4粉末变蓝,这说明有水蒸气生成,也就是白色固体中一定含有氢氧化镁,则猜想③成立;故填:③;(3)因为加热后生成了水蒸气和二氧化碳,所以要将生成气体先通过浓硫酸吸收生成的水蒸气;然后再通过浓氢氧化钠溶液吸收二氧化碳,否则会导致从氢氧化钠溶液中又带出部分水蒸气,造成误差;所以选择甲装置;故填:甲;
xMgCO3yMg(OH)23H2O | (x+y)MgO+(y+3)H2O+ | xCO2↑ |
40(x+y) | 44x | |
1.660g | 1.32g |
![]()
x:y=3:1
故填:3:1;(4)碱式碳酸镁与氢氧化钠反应生成氢氧化镁沉淀、碳酸钠和水;故填:3MgCO3Mg(OH)23H2O+6NaOH=4Mg(OH)2↓+3Na2CO3+3H2O;(5)a、可燃物的着火点是物质本身的属性,不会降低,故错误;
b、生成的固体覆盖燃烧物,隔绝氧气,故正确;
c、生成的气体稀释了可燃物周围的氧气浓度,故正确.
故填:bc.