题目内容
【题目】向一定质量的Ba(OH)2溶液中先后滴加CuSO4、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图所示.下列说法正确的是( ) 
A.a点对应溶液pH>7
B.b点对应溶液中溶质有2种
C.m=3.31
D.取c点对应溶液,滴加NaOH溶液,立刻产生沉淀
【答案】AC
【解析】解:A、通过图象可以看出,a所处的图象表示在滴加硫酸的过程中,沉淀的质量继续增大,所以a点对应的溶液中含有氢氧化钡,溶液pH>7,故A正确; B、b点所处的图象沉淀质量在减小,表示硫酸和氢氧化铜的反应,此时溶液中的溶质是硫酸铜一种,故B错误;
C、由图象中的数据可知,生成的氢氧化铜的质量为:5.64g﹣4.66g=0.98g,
硫酸铜和氢氧化钡反应生成的硫酸钡沉淀的质量为x
CuSO4+Ba(OH)2= | Cu(OH)2↓+ | BaSO4↓ |
98 | 233 | |
0.98g | x |
![]() =
= ![]()
x=2.33g
所以m=2.33g+0.98g=3.31g,故C正确;
D、取c点对应溶液,硫酸过量,滴加NaOH溶液,不能立刻产生沉淀,故D错误.
故选:AC.

 53随堂测系列答案
53随堂测系列答案【题目】氯化镁是一种重要的化工原料,同学们在实验室对其开展了系列研究.
(1)课题1:选择制取氯化镁的原料 【查阅资料】
①全球海水中含有的盐类总质量为5亿亿吨,其中含有的各种离子占盐类总质量的百分含量如下表所示:
离子 | Cl﹣ | Na+ | Mg2+ | Ca2+ | K+ | 其他 |
含量 | 55.06% | 30.61% | 3.69% | 1.15% | 1.10% | … |
②工业生产中海水或卤水(海水晒盐后的剩余溶液)都可以作为制取氯化镁的原料.
【交流讨论】
同学们经讨论,一致选择卤水用于实验室制取氯化镁.你认为他们的理由是 .
(2)课题2:由卤水制取氯化镁 同学们设计如图所示方案,从卤水中制取氯化镁.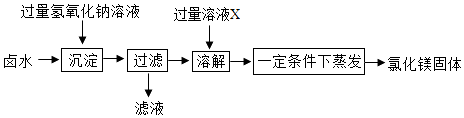
①溶液X的名称是 .
②部分同学认为上述制取方案不够完善,在“过滤”操作后缺少“洗涤”操作,从而导致制取的氯化镁不纯,可能混有的杂质是 .
(3)课题3:测定氯化镁产品的纯度(氯化镁的质量分数) 同学们设计如下实验方案对制得的氯化镁进行纯度测定.
【实验步骤】
①称取9.5g氯化镁样品,放于烧杯中,加足量的水溶解,形成溶液;
②向上述溶液中加入90g质量分数为10%的氢氧化钠溶液;
③充分反应后,过滤;
④…
⑤向所得溶液中加入几滴无色酚酞试液,溶液变红,再逐滴加入10%稀硫酸(密度为1.07gmL﹣1),并 , 当观察到溶液恰好褪色且30s内红色不复现,停止加入稀硫酸;
⑥计算氯化镁样品的纯度.
(4)【问题讨论】 ①为计算出氯化镁样品的纯度,除上述数据外,实验还需测量的数据是 .
②若缺少步骤④,则会导致氯化镁纯度测定不准确,步骤④的操作是 .