题目内容
【题目】发展利用太阳能可以推进节能减排。晶体硅是制造太阳能电池的重要原料。如图是工业上以石英砂(SiO2)为主要原料制取纯硅的一种方法,请回答下列问题(备注:粗硅中的主要成分是硅)
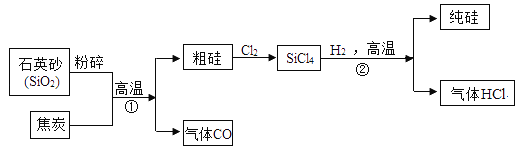
(1)将石英砂粉碎的目的是_______;
(2)焦炭在反应①中体现出来的化学性质是______;
(3)出步骤①中发生反应的化学方程式:_________;
(4)写出步骤②中发生反应的化学方程式:________;
(5)尾气氯化氢必须收集处理,不能排放到空气中,原因是_______。
【答案】与焦炭充分反应 还原性 SiO2+2C![]() Si+2CO↑ 2H2+SiCl4
Si+2CO↑ 2H2+SiCl4![]() Si+4HCl 氯化氢气体会污染空气
Si+4HCl 氯化氢气体会污染空气
【解析】
(1)将石英砂粉碎的目的是:增大与焦炭的接触面积,是反应更充分;
(2)焦炭在反应①中能夺取二氧化硅中的氧,体现出来的化学性质是还原性;
(3)反应①是碳和二氧化硅在高温下生成硅和一氧化碳,对应的化学方程式是:SiO2+2C![]() Si+2CO↑;
Si+2CO↑;
(4)由题意可知。在步骤②中四氯化硅和氢气在高温的条件下生成硅和氯化氢气体,方程式是:2H2+SiCl4![]() Si+4HCl;
Si+4HCl;
(5)尾气氯化氢必须收集处理,不能排放到空气中,原因是氯化氢会污染环境。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目