题目内容
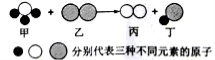
【题目】已知A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,G是一种重要建筑材料的主要成分,E是一种金属氧化物,与A反应能生成一种常见的碱。它们之间的转换关系如图所示:
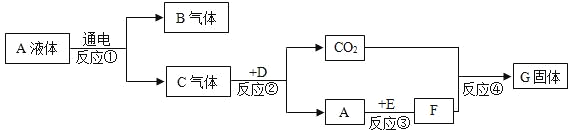
(1)写出下列物质的化学式:A_____、D_____。
(2)写出反应④的化学方程式_____。
(3)E在日常生活中用途广泛,请写出其中一点_____。
【答案】H2O CH4 Ca(OH)2+CO2=CaCO3↓+H2O 作食品干燥剂(其他合理即可)
【解析】
A在常温下是一种无色液体,且反应条件为通电的条件下生成BC两种气体,在初中只有水电解生成氢气和氧气,所以A为水,BC对应氧气和氢气之一;而D是天然气的主要成分,即为甲烷,能和C气体反应生成二氧化碳和A,所以C支持燃烧,所以C为氧气,B为氢气;G是一种重要建筑材料的主要成分的固体,所以为碳酸钙,则F为氢氧化钙,而E是一种金属氧化物,与A反应能生成一种常见的碱,为氢氧化钙,对应的E为氧化钙;所以A为水,B为氢气,C为氧气,D为甲烷,E为氧化钙,F为氢氧化钙,G为碳酸钙。
由分析可知:(1)由于A为水,对应的化学式为H2O;D为甲烷,对应的化学式为CH4;
(2)反应④是二氧化碳和氢氧化钙反应生成碳酸钙和水,对应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O;
(3)E是氧化钙,可以吸收水分,所以在日常生活中可用作食品干燥剂( 其他合理即可)。

 口算能手系列答案
口算能手系列答案【题目】(关注生活现象)
维生素C泡腾片可增强机体抵抗力,将其放入冷水或温开水中,立刻生成大量二氧化碳气体状如沸腾,并得到一杯美味的饮品,如表为维生素C泡腾片的部分成分及溶解性表。
主要成分 | 维生素C | 柠檬酸 | 碳酸氢钠 | 山梨醇 | 淀粉 | 二氧化硅 |
溶解性 | 易溶 | 易溶 | 易溶 | 易溶 | 难溶 | 难溶 |
请回答下列问题。
(1)维生素C泡腾片在冷水中的溶解速率比在温开水中_____(填“快”或“慢”)
(2)维生素C泡腾片放入水中溶解后能否得到溶液_____(填“能”或“否”),理由是_____。
(3)检验生成的二氧化碳的方法是(用化学方程式表示)_____。
【题目】化学与实验.
(一)气体的制取和收集
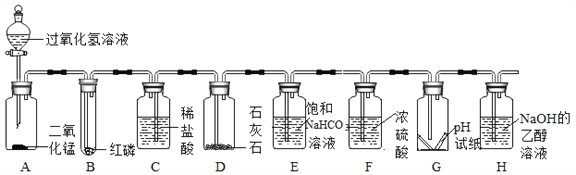
现有如图所示的实验装置:
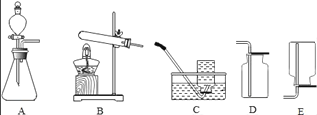
(1)A装置可用于制___气体,反应的化学方程式为:___.
(2)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得.制甲烷气的发生装置应选用___(填字母)装置;收集甲烷气可选用C或E装置,由此推断甲烷气具有的物理性质是___.
(3)实验室用A装置制取气体前,先向长颈漏斗中加水淹没长颈漏斗的下端,其目的是为了___.
(4)用B、D组合制取制氧气的化学方程式为___,检验氧气已集满的方法是___.
(二)某食品包装袋中有一个小纸袋,上面写“生石灰干燥剂,请勿食用”.该食品已放置两月有余.请你对下列问题进行探究.
(1)小纸袋中的物质能否继续作干燥剂?
实验步骤 | 实验现象 | 结论 |
取足量的小纸袋中的固体放入 烧杯中,加入适量的水,触摸杯壁 | ___ | 可继续作干燥剂 |
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和___;
(3)请设计实验证明(2)中你所填的物质是否存在___.
【题目】实验小组对过氧化氢的某些性质进行探究
(查阅资料)过氧化氢是一种受热易分解的物质,某些漂白液中含有过氧化氢溶液,过氧化氢溶液可漂白一些有色物质
(进行实验)
实验A:室温下用10%的过氧化氢溶液浸泡一块红色布条(如图所示),浸泡时间与布条颜色变化如下表
浸泡时间 | 20min | 40min | 60min |
布条颜色的变化 | 无明显变化 | 颜色稍变浅 | 颜色明显变浅 |
实验B:改变实验条件再进行4次实验,现象如下表
编号 | ① | ② | ③ | ④ |
实验条件 | 20℃25mL 10%H2O2溶液 | 50℃25mL 10%H2O2溶液 | 20℃25mL 10%H2O2溶液 +2mLNaOH溶液 | 50℃25mL 10%H2O2溶液 +2mLNaOH溶液 |
布条颜色的变化 (20min) | 无明显变化 | 颜色稍变浅 | 颜色稍变浅 | 颜色明显变浅 |
(1)实验A的结论是_____
(2)实验B中,欲得出“其他条件相同时,升高温度可使过氧化氢溶液的漂白性增强”的结论,需要对比实验_____(填编号)
(3)实验B中,通过对比②④,得出的结论是_____
(4)更多的实验结果表明,漂白液的使用温度不宜过高,推测其原因是_____