题目内容
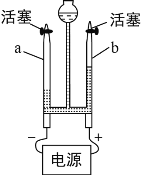
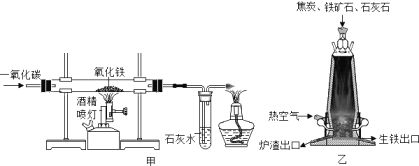
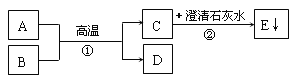
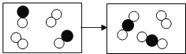
【题目】请根据下列实验装置图回答问题:
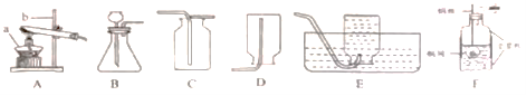
(1)仪器b的名称是____。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,发生反应的化学方程式为___________,用装置C收集氧气,证明集满的方法是________。
(3)实验室制取CO2,装置F是小亮制取CO2的气体发生装置,用它代替B装置的优点是________(答出一点即可)。
(4)加热氯化铵和熟石灰固体混合物制取NH3,可选用的发生装置是_______ (填字母序号),NH3只能用D装置收集,则NH3的物理性质__________。
【答案】铁架台 2H2O2![]() 2H2O + O2 ↑ 将带火星的木条将在集气瓶口,木条复燃 便于控制反应的开始和停止 A 密度小于空气,易溶于水
2H2O + O2 ↑ 将带火星的木条将在集气瓶口,木条复燃 便于控制反应的开始和停止 A 密度小于空气,易溶于水
【解析】
(1)据所学知识可知仪器b的名称是铁架台;
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,发生反应是过氧化氢在二氧化锰的作用下分解生成水和氧气,化学方程式为2H2O2 ![]() 2H2O+O2↑,用装置C收集氧气,证明集满的方法是将带火星的木条将在集气瓶口,木条复燃,证明已经集满氧气;
2H2O+O2↑,用装置C收集氧气,证明集满的方法是将带火星的木条将在集气瓶口,木条复燃,证明已经集满氧气;
(3)用装置F制取CO2的气体发生装置,将铜丝的下端伸入液面以下,固体反应物和液体反应物接触,反应开始,反之,反应停止。用它代替B装置的优点是便于控制反应的开始和停止;
(4)加热氯化铵和熟石灰固体混合物制取NH3,可选用的发生装置是固-固加热型A;选择收集装置需考虑气体的密度及是否与空气的成分反应、气体在水中的溶解性。密度比空气的大的气体,可以用向上排空气法收集,难溶于水的气体可以用排水法收集。NH3只能用D装置收集, 说明NH3的物理性质是密度小于空气,易溶于水。

【题目】实验室有一瓶配制数天的Na2SO3溶液,现在对其成分进行检测:
(成分猜想)猜想一:只有Na2SO3;
猜想二:_____;
猜想三:既有Na2SO3,也有Na2SO4。
(查阅资料)①Na2SO3易被空气中的氧气氧化生成Na2SO4.②BaSO4不溶于稀盐酸和稀硫酸。③Na2SO3和盐酸、硫酸反应均生成SO2。
(方案设计)
方案 | 实验操作 | 实验现象 | 结论 |
一 |
①加入足量的稀盐酸 ②再加入足量的BaCl2溶液 | _____ | 猜想三正确 |
二 | ①加入足 ②再加入足量的BaCl2溶液 | 有气体和白色沉淀生成 | 猜想一或猜想三正确 |
(方案分析)
(1)方案一中的实验现象为_____;方案一中加入BaCl2溶液后发生反应的化学方程式为_____。
(2)方案二的设计是否合理:_____(填“合理”或“不合理”);若不合理。理由是_____。
(实验结论)通过分析比较,方案设计_____(填“一”或“二”)合理。