题目内容
【题目】我国卫生部2012年启动首个“饮用水卫生宣传周”,其主题为“关注饮水卫生,共享健康生活”。城市自来水的生产过程大体如下图所示:
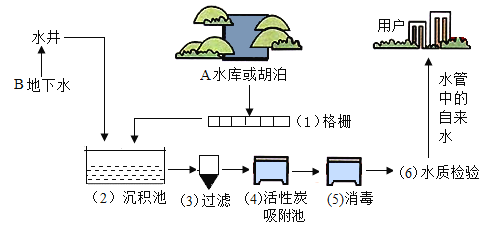
(1)自来水生产环节中的过滤池中有活性炭,活性炭起_____作用,该过程发生的_____变化。
(2)按新《标准》检测水质,从所取水样中检测出含氮、磷、钠等,这里的氮、磷、钠是指(____)
A 单质 B 分子 C 原子 D 元素
(3)二氧化氯是一种在水处理等方面有广泛应用的高效安全消毒剂,不会产生对人体有潜在危害的有机氯化物,则二氧化氯的化学式为_____,其中氯元素化合价为_____。
(4)高铁酸钾(化学式为K2FeO4)是一种集氧化、吸附、杀菌、灭藻、去浊、脱色、除臭为一体的新型高效水处理剂。下列关于高铁酸钾的叙述中正确的是(____)
A 高铁酸钾是一种氧化物 B 高铁酸钾的组成中含有两种非金属元素
C 高铁酸钾是一种混合物 D 高铁酸钾中铁元素的化合价为+6
【答案】吸附 物理 D ClO2 +4 D
【解析】
(1)活性炭具有吸附作用,吸附过程中没有新物质生成,属于物理变化;故答案为:吸附;物理。
(2)水样中的氮、磷、钠指的是元素,故答案为:元素。
(3)根据读法即可写出二氧化氯的化学式为ClO2,又因为氧元素为-2价,所以氯元素的化合价为+4价。故答案为:ClO2;+4。
(4)A、高铁酸钾中含有3种元素,属于化合物,A错误;B、高铁酸钾的组成中存在一种非金属元素(氧元素),B错误;C、高铁酸钾可以用化学式表示出来,说明是属于纯净物,C错误;D、高铁酸钾中钾元素的化合价为+1价,氧元素的化合价为-2价,根据化合物中各元素化合价的代数和为0,设铁元素的化合价为x,则![]() ,得x= 6,所以铁元素的化合价为+6价,D正确;故选D。
,得x= 6,所以铁元素的化合价为+6价,D正确;故选D。

【题目】用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15克干燥样品进行实验。
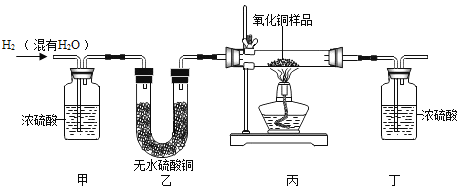
(1)实验中,乙装置的作用是_____。
(2)准确称取完全反应前后装置丙和丁的质量如表:
装置丙 | 装置丁 | |
反应前 | 48.8克 | 161.2克 |
反应后 | 46.5克 | 163.9克 |
小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度_____(写出计算过程)。
(3)根据以下原因计算,可能导致结果偏大的是_____。
A 装置的气密性不好
B 空气中的水分被丁处浓硫酸吸收
C 通入的氢气量不足
D 空气中的二氧化碳被丁处浓硫酸吸收