【题目】食盐、碳酸钠和碳酸氢钠是生活中常见的钠盐。请回答下列问题。
(1)碳酸氢钠的水溶液显_____性(填“酸”、“碱”或“中”)。碳酸氢钙受热易分解,碳酸氢钠性质与其相似,除去碳酸钠固体中混有的少量碳酸氢钠,反应的化学方程式为_______________________________。
(2)等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成的CO2量,前者_____后者(填“>”、“<”或“=”)。
(3)粗盐含有少量杂质(主要为CaCl2、MgCl2、Na2SO4等)。用粗盐制取“化学纯”级的NaCl,步骤为溶解、加过量a、加过量NaOH、加过量b、过滤、加适量盐酸,蒸发结晶得到“化学纯”级的NaCl固体。试剂a、b分别是_____(填序号)
A Na2CO3、BaCl2 B BaCl2、Na2CO3 C BaCl2、Na2SO4
(4)工业上用电解饱和食盐水的方法生成氯气和烧碱。
资料一:Cl2+H2O=HCl+HClO
资料二:初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣=H2O,像这种用实际参加反应的离子符号来表示反应的式子叫离子反应,离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
①写出Na2SO4与BaCl2反应的化学方程式:_________________________
②把易溶于水,易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示,上述化学方程式可改写成,2Na++SO42﹣+Ba2++2Cl﹣=BaSO4↓+2Na++2Cl﹣
③删去方程两边不参加反应的离子:Ba2++SO42﹣=BaSO4↓:
④检查方程式两边各元素的原子个数和电荷总数是否相等
⑤某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理________________________(用离子方程式表示)
资料三:化学反应类型有不同的分法,其中反应前后,有元素化合价变化的化学反应是氧化还原反应。氧化还原反应中有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂,化合价没有发生变化的既不是氧化剂也不是还原剂。
⑥工业上可用氨检验输送氯气的管道是否漏气。反应方程式如下:8NH3+3Cl2=6NH4Cl+N2,该反应_____(填“是”或“不是”)氧化还原反应,其中氧化剂和还原剂物质的量之比为__________(若是氧化还原反应,此空作答,反之,不作答)
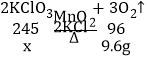
![]() x=24.5g
x=24.5g![]()