题目内容
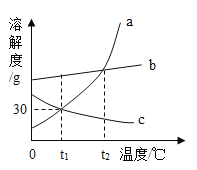
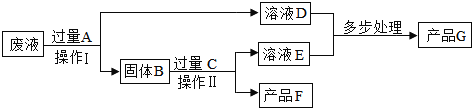
【题目】(关注生产实际)为提高农作物产量,现代农业生产需施用一定量化肥,某化肥厂生产化肥的流程如下:(已知10℃时K2SO4的溶解度为9.3g,NH4Cl的溶解度为33.3g)
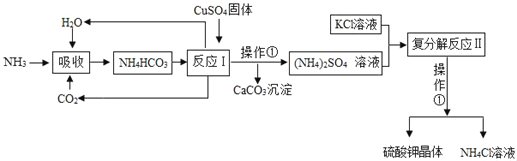
(1)操作①的名称是___。
(2)吸收过程中所发生反应的化学方程式:___。
(3)NH4HCO3中氮元素的化合价为___。
(4)在生产流程中可回收利用的物质有___。
(5)复分解反应Ⅱ的发生温度需控制在10℃的原因是___。
【答案】过滤 NH3+H2O+CO2=NH4HCO3 ﹣3价 二氧化碳和水 该温度下硫酸钾的溶解度很小,视为不溶,该反应才能发生
【解析】
(1)操作①实现了固体和液体的分离,为过滤。
(2)吸收过程中是氨气和二氧化碳以及水反应生成碳酸氢铵,对应的化学方程式:NH3+H2O+CO2=NH4HCO3。
(3)NH4HCO3中氮元素在铵根中,由于铵根为+1价的,而氢元素为+1价,所以对应的氮元素的化合价为﹣3价。
(4)开始二氧化碳和水都是反应物,而后来生成二氧化碳和水,所以在生产流程中可回收利用的物质有二氧化碳和水。
(5)由于复分解反应的条件中生成物必须有气体或者沉淀或者是水之一,而氯化铵和硫酸钾常温下溶解度很大,而只有10℃下硫酸钾的溶解度很小,视为不溶,该反应才能发生,所以复分解反应Ⅱ的发生温度需控制在10℃。

【题目】在实验室里加热氯酸钾(KClO3)和二氧化锰的混合物制取氧气,实验测得试管中固体的质量随时间变化的相关数据见下表:请通过计算回答:
加热时间/min | 0 | t1 | t2 | t3 | t4 |
固体质量/g | 28.0 | 25.4 | 23.2 | 18.4 | 18.4 |
请请通过计算回答:
(1)实验过程中共制得氧气_____g;
(2)当完全反应后,二氧化锰的质量为_____g;
(3)原混合物中氯酸钾的质量分数___?(写出计算过程)
【题目】(1)某化学课外兴趣小组对草酸分解生成物中碳的氧化物种类进行了如下实验探究:
(提出问题)生成物中有哪几种碳的氧化物?
(猜测)
猜想1 | 猜想2 | 猜想3 |
只有CO | 只有 | 含有CO和CO2 |
(设计实验)基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如下实验:
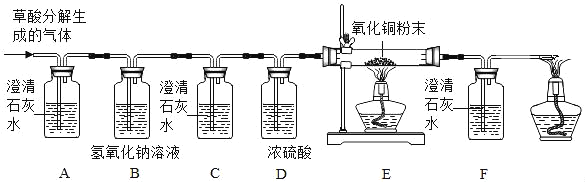
(实验探究)
(1)观察到装置_____(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成。
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置中澄清石灰水不变浑浊,F装置中_____;
②E装置中出现_____的现象。
(实验结论)通过实验探究证明:猜测3成立。
草酸分解的化学方程式是_____。
(问题讨论)
(1)B装置的作用是_____。
(2)装置末端酒精灯的作用是_____。